Пластика грыжи по ramirez

Правильный хирургический подход к пластике больших и гигантских вентральных грыж все еще является предметом дискуссий из-за высокой периоперационной заболеваемости (увеличение внутрибрюшного давления с исходом в компартмент-синдром, дыхательная недостаточность и др.), частых рецидивов и ухудшения качества жизни. Европейская ассоциация герниологов вовсе говорит о том, что значительные дефекты брюшной стенки являются большой проблемой как для хирурга, так и для пациента. Также их устранение служит серьезной задачей с точки зрения надежности и долговременности.
Метод восстановления Rives-Stoppa разрабатывался как эффективное восстановление с благоприятными исходами и низкой заболеваемостью. Диссекция фасции прямой мышцы живота обеспечивает высвобождение и мобильность самой мышцы и создает хорошо васкуляризированный «ящик» для размещения сетчатого имплантата. Но эта процедура не подходит для крупных дефектов из-за часто возникающей невозможности переднего фасциального закрытия, что приводит к тому, что большая поверхность сетки располагается под кожей. Непосредственным результатом является увеличение частоты случаев хирургического вмешательства и инфекций в месте хирургического вмешательства.
Сепарация переднего компонента (ACS), описанная Рамирезом, несмотря на улучшение результатов, обременена значительным размером раны. Это растягивает процесс восстановления, усиливает болевой синдром и увеличивает вероятность возникновения послеоперационных осложнений. Минимально инвазивные хирургические модификации уменьшали раневую поверхность, но не могли улучшить частоту рецидивов, которая все еще составляет до 30 % .
В 2012 году был разработан новый подход к разделению заднего компонента с помощью высвобождения поперечных мышц живота (Transversus Abdominis Muscle Release, TAR). Это модификация метода Rives-Stoppa с созданием широкого пространства между поперечной мышцей живота (transversus abdominis), поперечной фасцией и брюшиной.
Приведем пошаговую методику TAR-пластики на примере послеоперационной вентральной грыжи:
1. Срединная лапаротомия с полным удалением рубца. Пупок обычно иссекают. Грыжевой мешок рассекается, как при любой другой грыже.
2. Адгезиолизис. Кишечник и сальник освобождаются от задней поверхности передней брюшной стенки, чтобы обеспечить медиализацию этого слоя и предотвратить повреждения кишечника во время реконструкции.
3. Создание ретроректального пространства начинается на уровне пупка. Разрез производят на задней части фасции прямой мышцы живота на 0,5–1 см медиальнее латерального края.
Рисунок 1
Разрез фасции прямой мышцы с открытием и созданием ретромышечного пространства. Важнейшим этапом процедуры является идентификация самой прямой мышцы. Пунктирная линия — линия разреза по задней поверхности прямой мышцы.
NB! Важно не допустить «проваливания» прямой мышцы живота в брюшную плоскость!
Разрез расширяется краниально и каудально по всей длине фасции прямой мышцы, а получившееся пространство расширяется тупым способом. Латерально диссекция распространяется на полулунную линию. Необходимо позаботиться о том, чтобы предотвратить повреждения эпигастральных сосудов и сосудисто-нервных пучков прямой мышцы, которые перфорируют ее заднюю оболочку медиально к спигелиевой линии (рис. 2).
Ретромышечное пространство продолжается рассечением фасции краниально до мечевидного отростка и каудально практически до лобкового симфиза.
4. В верхней трети передней брюшной стенке производится разрез по задней поверхности прямой мышцы живота на 0,5 см медиальнее перфорирующих ее нервов. Задний листок фасции прямой мышцы живота надсекается, чтобы обнажить нижележащую поперечную мышцу (рис. 2).
Рисунок 2
Создание ретромышечного пространства. Рассечение расширено латерально до полулунной линии (желтая стрелка), где можно легко идентифицировать нервы и сосуды прямой мышцы живота
Как только мышца визуализируется, ее волокна разделяются по всему медиальному краю. Отделение от предбрюшинного пространства легко осуществляется с помощью L-изогнутого диссектора (рис. 3). В верхней трети мышца хорошо развита и ее легко идентифицировать.
Рисунок 3
После рассечения ретроректального пространства поперечная мышца рассекается на 0,5 см медиальнее полулунных линий (пунктирная стрелка). Разрез проводят по всей его длине (пунктирная линия) медиальнее нервов и сосудов (желтая стрелка).
5. Создание преперитонеального пространства: вертикально расслаиваются поперечные мышцы и сводятся их края. Во время создания плоскости могут произойти разрывы брюшины. Все они должны быть тщательно закрыты рассасывающимися нитями (обычно викрил 3/0), чтобы избежать выпячивания тонкой кишки под сеткой. В редких случаях (2 %) большие разрывы брюшины не могут быть закрыты и должны быть подкреплены сальником, местным жиром или даже абсорбируемой сеткой. В боковом направлении расслоение простирается до поясничной мышцы: его боковая граница может использоваться в качестве ориентира, хотя обычно основным анатомическим ориентиром для бокового рассечения является задняя подмышечная линия (рис. 4).
Рисунок 4
Рассечение поперечной мышцы живота. Желтая стрелка — волокна поперечной мышцы.
6. Соединение заднего листка фасции прямой мышцы с помощью медленно рассасывающейся нити.
7. Перед размещением сетки получившееся широкое предбрюшинное пространство измеряется по длине и ширине для моделирования сетчатого имплантата. Обычно необходима сетка размером более 30/30 см. Используется полипропиленовая сетка из моноволокна с крупными порами с низкой или средней массой (от 40 до 60 г/м2). Для боковых или очень больших дефектов может потребоваться более тяжелая сетка. Сетка должна перекрывать дефект как минимум до передней подмышечной линии, субксифоидального пространства и лобкового симфиза.
8. Первым шагом крепления сетки является сшивание сетки с обеими связками Купера. Низкая фиксация необходима для защиты надлобковой области, потому что векторы внутрибрюшного давления направлены вниз. Краниально двумя швами фиксируют сетку вокруг мечевидного отростка, покрывая эпигастральную область. Сетка может быть зафиксирована в ретромускулярном пространстве с помощью биологического клея с лучшими результатами в плане послеоперационной боли и восстановления. Пространство и сетка орошаются солевым раствором с гентамицином.
После окончания основного этапа операции около сетки устанавливаются два дренажа и послойно ушивается передняя брюшная стенка.
Источники:
1. Novitsky YW, Porter JR, Rucho ZC, Getz SB, Pratt BL, Kercher KW, et al. Open preperitoneal retrofascial mesh repair for multiply recurrent ventral incisional hernias. J Am Coll Surg. 2006; 203(3):283-9. Epub 2006 Jul 13.
2. Ramirez OM, Ruas E, Dellon AL. “Components separation” method for closure of abdominal wall defects: an anatomic and clinical study. Plast Reconstr Surg. 1990 Sep;86(3):519-26.
3. Saulis AS, Dumanian GA. Periumbilical rectus abdominis perforator preservation significantly reduces superficial wound complications in “separation of parts” hernia repairs. Plast Reconstr Surg. 2002;109(7):2275-80; discussion 2281-2.
4. Fox M, Cannon RM, Egger M, Spate K, Kehdy FJ. Laparoscopic component separation reduces postoperative wound complications but does not alter recurrence rates in complex hernia repairs. Am J Surg. 2013;206(6):869-74; discussion 874-5. doi: 10.1016/j.amjsurg.2013.08.005. Epub 2013 Oct 7.
5. Georgiev-Hristov T, Celdrán A. Comment to: A systematic review of the surgical treatment of large incisional hernia. Deerenberg EB, Timmermans L, Hogerzeil DP, Slieker JC, Eilers PH, Jeekel J, Lange JF. Hernia 2015; 19:89-101. Hernia. 2015 Dec;19(6):1019-20. doi: 10.1007/s10029-015-1393-2.Epub 2015 May 30.
6. Novitsky YW, Elliot HL, Orenstein SB, Rosen MJ. Transversus abdominis muscle release: a novel approach to posterior component separation during complex abdominal wall reconstruction
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
ОПЕРАЦИЯ RAMIREZ II В УСЛОВИЯХ ОСТРОГО ЭКСПЕРИМЕНТА
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Паршиков В.В.
1, 2
Зарубенко П.А.
1
Базаев А.В.
1, 3
Топчубаев Д.Э.
1
Кошельник Т.С.
1
Хазова К.Д.
1
1 ФГБОУ ВО «Приволжский исследовательский медицинский университет» Минздрава РФ
2 Городская больница №35 Нижнего Новгорода
3 ГБУЗ НО «НОКБ им. Н.А. Семашко»
В условиях острого эксперимента моделировали операцию Ramirez II на 17 кроликах. Создавали дефект длиной 15 см и шириной 5 см путем иссечения тканей брюшной стенки, далее выполняли переднюю сепарацию в варианте Ramirez II. Применяли эндопротезы из стандартного полипропилена. Сетками протезировали как медиальный сегмент брюшной стенки, так и латеральные зоны разделения компонентов последней. Измеряли геометрические параметры брюшной стенки, создаваемого в последней отверстия, окружность талии животного, продолжительность операции и внутрибрюшное давление (ВБД). Операция в среднем длилась 114,88 мин, интерквартильный размах (ИКР) 100–121 мин. Площадь передней брюшной стенки составила 265,65 см2, ИКР 228–283,5 см2. Соотношение площадей дефекта и передней стенки живота оказалось 23,01%, (ИКР 20,77–25,82%), ВБД после реконструкции брюшной стенки составило 6,25 мм рт. ст. (ИКР 5,2–7,4) Обнаружили сильную прямую корреляцию между окружностью талии животного и площадью его переднебоковой стенки живота. В настоящем исследовании впервые моделирована передняя сепарационная протезирующая пластика в варианте Ramirez II у кроликов. Изучили возможность и особенности техники осуществления данного вида вмешательства. Оценили сложность выполнения оперативных приемов на определенных этапах. В ходе работы стандартизированы технические навыки, алгоритм действий хирургической бригады и обоснована возможность использования рассмотренной модели для выполнения хронического эксперимента.
большие грыжи
сепарация
протезирующая пластика
сетка
эксперимент
ramirez
1. Petersson P., Montgomery A., Petersson U. Modified peritoneal flap hernioplasty versus retromuscular technique for incisional hernia repair: a retrospective cohort study. Scandinavian Journal of Surgery. 2019. P. 1457496919863943.
2. Lindmark M. Strigård, K., Löwenmark, T., Dahlstrand, U., Gunnarsson U. Risk factors for surgical complications in ventral hernia repair. World Journal of Surgery. 2018. vol. 42. no. 11. P. 3528-3536.
3. Thankam F.G., Palanikumar G., Fitzgibbons R.J., Agrawal D.K. Molecular mechanisms and potential therapeutic targets in incisional hernia. Journal of Surgical Research. 2019. vol. 236. P. 134–143.
4. Bellio G., Cipolat Mis T., Del Giudice R., Munegato G. Preoperative abdominal computed tomography at rest and during Valsalva’s maneuver to evaluate incisional hernias. Surgical Innovation. 2019. P. 1553350619849986.
5. Sakamoto Y., Yamada M., Yamada Y., Yokoyama Y., Kishi K., Jinzaki M. Use of CT in a standing position for preoperative evaluation in abdominal incisional hernia: A pilot study. J. Plast. Reconstr. Aesthet. Surg. 2019. vol. 72. no. 12. Р. e1-e2.
6. Winters H., Knaapen L., Buyne O.R., Hummelink S., Ulrich D.J.O., van Goor H., van Geffen E., Slater N.J. Pre-operative CT scan measurements for predicting complications in patients undergoing complex ventral hernia repair using the component separation technique. Hernia. 2019. vol. 23. no. 2. P. 347-354.
7. Arslan U., Bilecik T. Is component separation a safe method in incisional hernias? Istanbul Medical Journal. 2019. vol. 20. no. 4. P. 342-346.
8. Maloney S.R., Schlosser K.A., Prasad T., Kasten K.R., Gersin K.S., Colavita P.D., Kercher K.W., Augenstein V.A., Heniford B.T. Twelve years of component separation technique in abdominal wall reconstruction. Surgery. 2019. vol. 166. no. 4. P. 435-444.
9. Sneiders D., Yurtkap Y., Kroese L.F., Jeekel J., Muysoms F.E., Kleinrensink G.J., Lange J.F. Anatomical study comparing medialization after Rives-Stoppa, anterior component separation, and posterior component separation. Surgery. 2019. vol. 165. no. 5. P. 996-1002.
10. Гребцов Ю. В., Луговой А.Л., Накопия Г.Г. Первый опыт пластики брюшной стенки с разделением ее компонентов и применением сетчатого импланта по поводу послеоперационных вентральных грыж // Здоровье – основа человеческого потенциала: проблемы и пути их решения. 2016. №. 2. С. 690-691.
11. Егиев В.Н., Кулиев С.А., Евсюкова И.В. Первые результаты после передней сепарационной пластики у пациентов со срединными грыжами // Здоровье и образование в XXI веке. 2017. Т. 19. №. 8. С. 18-20.
12. Коробейникова Е.П., Комарова Е.Ф. Лабораторные животные – биомодели и тест–системы в фундаментальных и доклинических экспериментах в соответствии со стандартами надлежащей лабораторной практики (НЛП/GLP) // Журнал фундаментальной медицины и биологии. 2016. №1. С. 30–36.
13. Yoshino O., Quail A., Oldmeadow C., Balogh Z.J. The interpretation of intra-abdominal pressures from animal models: the rabbit to human example. Injury. 2012. vol. 43. no. 2. P. 169-173.
Несмотря на активное внедрение протезирующей пластики, совершенствование оперативной техники и вариантов размещения сетки, проблема эффективного лечения пациентов c грыжами больших размеров далека от своего решения [1]. Сохраняется высокая частота послеоперационных осложнений и рецидивов заболевания в данной категории больных [2]. Во многом это связано с формирующимися анатомическими и функциональными изменениями живота [3]. По данным компьютерной томографии у ряда пациентов с большими грыжами определяются редукция объема брюшной полости (loss of domain) и неполноценность мышечного каркаса брюшной стенки [4–6]. Данная категория пациентов нуждается в особом подходе, предоперационной подготовке, коррекции сопутствующей патологии и применении современных возможностей оперативного лечения. Для реконструкции брюшной стенки разработаны методы, в основе которых лежит техника разделения компонентов, использование которой позволяет успешно завершить пластику в ситуации потери домена [7, 8]. Принято различать переднюю (anterior components separation technique – ACST) и заднюю (posterior components separation technique – PCST) сепарацию [9]. В российских клиниках применение передней сепарационной пластики остается редким. Например, использование техники Ramirez описано в работе 2016 г. у 2 пациентов [10] и в публикации 2017 г. у 40 пациентов [11]. Это связано с техническими сложностями и недостаточным опытом проведения передних сепарационных пластик у большинства хирургов, высоким риском развития послеоперационных осложнений, а также с отсутствием рандомизированных контролируемых исследований с большим размером выборки и последующим длительным наблюдением. Несмотря на актуальность и сложность рассматриваемой проблемы, неоднозначность мнений экспертов, ограниченность и противоречивость клинических данных, при изучении литературы мы не нашли исследований ACST на экспериментальных животных.
Цель исследования: оценить техническую возможность и изучить особенности выполнения операции Ramirez II в остром эксперименте.
Материал и методы исследования. Работа выполнена в рамках вариативного цикла «Экспериментальная хирургия» на базе кафедры общей, оперативной хирургии и топографической анатомии им. А.И. Кожевникова на 17 половозрелых кроликах породы «Калифорнийский» и «Русская шиншилла» разного пола, массой 2,5–7 кг с разрешения локального этического комитета – протокол № 7 от 05.07.2018 г. Исследование проведено в соответствии с законодательством РФ («Правила гуманного обращения с лабораторными животными», «Деонтология медико-биологического эксперимента») и концепцией 3R (reduction, refinement, replacement), актуальной в экспериментальной хирургии и биологии [12]. В остром эксперименте создавали дефект брюшной стенки 5 см шириной и 15 см длиной. Операции выполнены в условиях общей анестезии препаратами Золетил 100 (25 мг/кг) и Ксилавет (3 мг/кг) внутримышечно. Животным проводили измерение длины паховой связки, реберной дуги до задней подмышечной линии, определяли расстояние от мечевидного отростка до симфиза, а также между концами 11 ребер и передними остями подвздошных гребней, окружность талии. Вычисляли площади передней стенки живота и грыжевого дефекта. Измеряли продолжительность оперативного вмешательства, внутрибрюшное давление (ВБД) – исходное и после ACST – аналогично I. Kron Последовательность этапов операции соответствовала передней сепарационной пластике Ramirez II. Рассекали кожу и клетчатку в проекции белой линии живота. Латеральнее последней на 2 мм осуществляли доступ во влагалища прямых мышц на протяжении 18–20 см билатерально. Создавали дефект 15х5 см, для этого иссекали задний влагалищный листок вместе с брюшиной (рис. 1). Далее выполняли препаровку в ретромускулярном пространстве (рис. 2). Затем производили диссекцию в подкожном слое, отступив 5 мм от латерального края прямой мышцы, проводили продольный разрез апоневроза наружной косой мышцы длиной до 18 см (рис. 3) и выполняли сепарацию между наружной и внутренней косыми мышцами в латеральном направлении до поясничных сосудов, что составляло около 6 см. Все этапы последовательно осуществляли билатерально. Края грыжевого дефекта ушивали непрерывным швом викрилом 2/0 (рис. 4). На восстановленный задний листок укладывали сетку, которую фиксировали узловыми швами викрилом 4/0 в двух местах. Затем укрепляли боковые поверхности живота, укладывая сетки в форме полуэллипса между наружной и внутренней косыми мышцами (рис. 5). Медиальный широкий край эндопротеза фиксировали узловыми швами викрилом 4/0 к латеральному краю прямой мышцы, а отсеченный край наружной косой мышцы фиксировали к латеральному полуовальному краю сетки. Ушивали передние листки влагалищ прямых мышц живота непрерывным швом нитью Monoplus 2/0, восстанавливая их медиальное анатомическое положение (рис. 6). Послойно ушивали рану. Этапы вмешательства показаны на рисунках 1–6. Для выведения животных из эксперимента применяли способ воздушной эмболии 7 мл/кг в краевую вену уха под наркозом. Результаты эксперимента обрабатывали средствами Statistica 10.0. Распределение количественных данных изучали методом Shapiro–Wilk. Использовали t-критерий Wilcoxon в зависимых выборках и тест Mann–Whitney – в независимых. При анализе количественных данных применяли корреляционный анализ Spearmen для выявления взаимосвязи с целью определения силы и направления последней использовали шкалу Чеддока. Различия считали статистически значимыми при p <0,05.
|
|
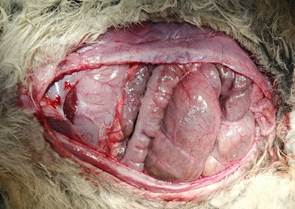
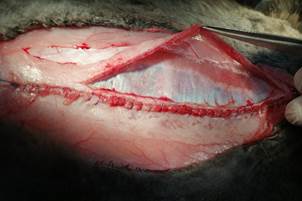
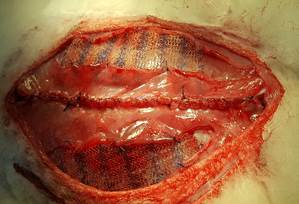
Рис. 1. Создание дефекта брюшной стенки | Рис. 2. Ретромускулярная диссекция. Пинцетом захвачена прямая мышца, рассечен апоневроз наружной косой |
|
|
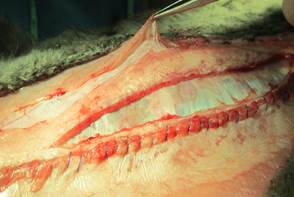
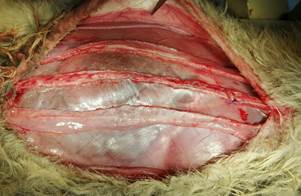
Рис. 3. Начало диссекции в наружных слоях передней брюшной стенки. Пинцетом захвачена наружная косая мышца | Рис. 4. Выполнена диссекция в ретромускулярном пространстве и в боковых областях живота. Задние листки влагалищ ушиты непрерывно |
|
|
Рис. 5. Размещение сеток, их фиксация и шов передних листков влагалищ прямых мышц | Рис. 6. Белая линия восстановлена, прямые мышцы аппроксимированы в их естественной медиальной позиции |
Результаты исследования и их обсуждение. В результате эксперимента установлено, что выполнение передней сепарационной пластики на кролике вполне возможно. Тем не менее имелись технические трудности на определенных этапах, связанные как с особенностями анатомии передней брюшной стенки кролика, так и с опытом и мануальными навыками оператора. Площадь грыжевого дефекта у каждого животного была стандартной и составляла 58,875 см2. Данные отражены в таблице 1.
Таблица 1
Данные эксперимента
Измеренные параметры | Min | Q1 | Median | Mean | SD | Q3 | Max |
Масса животного, кг | 2,5 | 3 | 3 | 3,5 | 1,04 | 3,5 | 7 |
Исходная окружность талии, см | 26 | 31 | 33 | 34,35 | 4,99 | 37 | 46 |
Окружность талии после операции, см | 26 | 30 | 33 | 33,18 | 4,79 | 35 | 45 |
Уменьшение объема талии в см | 1 | 1,18 | 0,95 | 2 | 3 | ||
Площадь брюшной стенки, см2 | 194 | 228 | 249,5 | 265,65 | 57,95 | 283,5 | 423,5 |
Отношение площадей дефекта и передней брюшной стенки, % | 13,9 | 20,77 | 23,59 | 23,01 | 4,28 | 25,82 | 30,35 |
ВБД до операции, мм рт. ст. | 2,9 | 3,8 | 4,4 | 4,16 | 0,76 | 4,4 | 5,5 |
ВБД после операции, мм рт. ст. | 4,4 | 5,2 | 5,9 | 6,25 | 1,28 | 7,4 | 8,8 |
Увеличение ВБД, мм рт. ст. | 0,6 | 1,5 | 2,1 | 2,09 | 1,13 | 3 | 4,5 |
Длительность операции, мин | 85 | 100 | 120 | 114,88 | 16,99 | 121 | 150 |
Примечание. Min – минимальное значение; Q1 – первый квартиль; Median – медиана; Mean – среднее арифметическое; SD – стандартное отклонение; Q3 – третий квартиль; Max – максимальное значение.
Выявлено статистически значимое уменьшение объема талии после операции в среднем на 1,18 см с интерквартильным размахом (ИКР 0–2 см), Т-критерий Wilcoxon р=0,002218. Результаты отражены на рисунке 7. Установлено повышение внутрибрюшного давления ВБД после передней сепарационной пластики в среднем на 2,09 мм рт. ст., ИКР 1,5–3 мм рт. ст., Т-критерий Wilcoxon р=0,000293 (рис. 8). По шкале Чеддока обнаружена сильная прямая корреляционная взаимосвязь: чем больше объем талии животного, тем больше площадь передней брюшной стенки, коэффициент корреляции Spearmen r=0,911019 при р=0,00000. Установлена умеренная прямая взаимосвязь между массой животного и площадью передней стенки живота, коэффициент корреляции Spearmen r=0,634235 при р=0,00001.
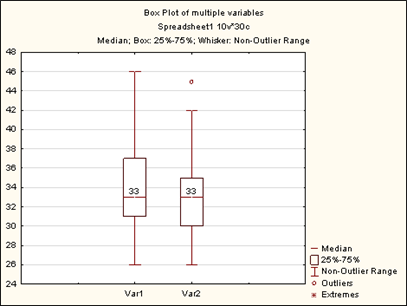
Рис. 7. Изменение объема талии животных в ходе эксперимента
По горизонтали: Var 1– объем талии животного до эксперимента медиана 33 см (ИКР 31–37 см); Var 2 – объем талии животного после эксперимента медиана 33 см (ИКР 30–35 см), по вертикали в см
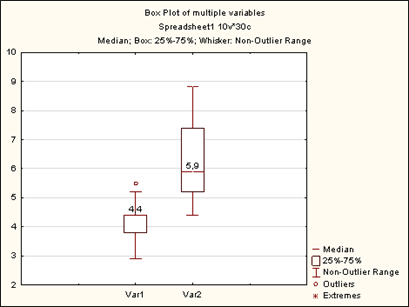
Рис. 8. Динамика ВБД в ходе эксперимента
По горизонтали: Var 1 – ВБД до эксперимента медиана 4,4 мм рт. ст. (ИКР 3,8–4,4 мм рт. ст.); Var 2 – ВБД после эксперимента медиана 5,9 мм рт. ст. (ИКР 5,2–7,4 мм рт. ст.), по вертикали шкала в мм рт. ст.
Рассмотренная модель ACST не только подходит для отработки и дальнейшего изучения данного вмешательства, но и может использоваться в учебных целях для совершенствования техники операции шаг за шагом, возможности работать с живыми тканями, позволяет видеть ошибки и исправлять их в ходе операции. Ранее зарубежные авторы изучили эластичность брюшной стенки кролика и человека [13]. Продемонстрирована взаимосвязь, позволяющая сопоставить ВБД кролика и человека. Выявлено, что стенки живота исследуемого объекта более эластичны, чем у человека. ВБД в нашем исследовании после операции Ramirez II в среднем составляло 6,25 мм рт. ст., что соответствует ВБД человека 12,3 мм рт. ст. (граница внутрибрюшной гипертензии) [14]. По анатомическому строению передняя брюшная стенка кролика в целом соответствует человеческой, но имеются особенности. Присутствует дополнительный мышечный слой – большая подкожная мышца (musculus subcutaneous). Последняя располагается непосредственно под кожей и простирается от шеи до паховых связок, а по бокам – до лопаток и боковых поверхностей живота. Из-за тонкого мышечного каркаса, где толщина каждой мышцы живота не более 1 мм, выполнение ретромускулярной диссекции было проблематичным. Особенно тонким оказался задний листок влагалища прямой мышцы ниже дугообразной линии, что иногда при неверном движении инструментом приводило к перфорации и проникновению в брюшную полость или повреждению эпигастральной артерии.
Заключение
В рамках настоящей работы впервые была выполнена операция Ramirez II у кроликов. Выбранная модель обладает достаточным размером передней брюшной стенки, ее строение соответствует строению таковой у человека. Продемонстрирована возможность и изучены особенности экспериментальной передней сепарации. Дана оценка сложности выполнения данного оперативного вмешательства на определенных этапах и его продолжительности, изучена динамика внутрибрюшного давления. Получены навыки выполнения ACST step by step. Следует полагать, что описанная модель может быть использована для дальнейшего изучения передней сепарационной пластики с целью закрытия больших грыжевых дефектов в хроническом эксперименте.
Библиографическая ссылка
Паршиков В.В., Зарубенко П.А., Базаев А.В., Топчубаев Д.Э., Кошельник Т.С., Хазова К.Д. ОПЕРАЦИЯ RAMIREZ II В УСЛОВИЯХ ОСТРОГО ЭКСПЕРИМЕНТА // Современные проблемы науки и образования. – 2020. – № 3.;
URL: https://science-education.ru/ru/article/view?id=29733 (дата обращения: 28.11.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник