Недержание при грыже позвоночника
Статья посвящена проблеме нейрогенных расстройств мочеиспускания при травме позвоночника и спинного мозга
Путь пациента с осложненной травмой позвоночника, т. е. сопровождающейся повреждением спинного мозга, начинается с нейрохирургического оперативного вмешательства и продолжается многоэтапной реабилитацией, направленной на коррекцию сопутствующих осложнений и восстановление утраченных функций организма [1]. Для таких больных есть специфический термин – «спинальные».
Одним из тяжелейших последствий травмы спинного мозга является расстройство произвольного мочеиспускания, обусловленное нарушением проводимости спинномозговых путей. По данным М.Р. Касаткина, подобное осложнение встречается в 92,1% случаев закрытых повреждений спинного мозга [2]. Патогенез изменений функции нижних мочевых путей при травме спинного мозга, проявляющийся в утрате рефлекторной деятельности, сложен и многообразен [3].
Механизм нормального мочеиспускания и характер его расстройства у спинальных пациентов напрямую связаны с особенностями физиологии этой области. Периферическую иннервацию нижних мочевых путей осуществляют тазовый нерв, представляющий парасимпатическую нервную систему, гипогастральный нерв, реализующий симпатическую регуляцию, и пудендальный соматический нерв. Афферентную информацию несут волокна всех трех нервов – вегетативных от детрузора (гладкой мышцы мочевого пузыря) и уретры и полового нерва от тканей промежности. Первичным анализатором для парасимпатического тазового нерва являются нейроны сакрального центра мочеиспускания, расположенного на уровне S2‒S4 сегментов спинного мозга. Здесь же, в анатомическом соседстве, находится ядро Онуфа, представляющее собой скопление нервных клеток, аксоны которых образуют пудендальный нерв [4]. Симпатическая афферентная иннервация, опосредованная гипогастральным нервом, являющимся частью подчревного и поясничного сплетения, осуществляется через пограничный симпатический ствол и вставочные интернейроны боковых рогов спинного мозга на уровне его Th10‒L2 сегментов. Эти же нервы несут и эфферентные сигналы к иннервируемым органам. Регулирующие структуры спинного мозга связаны с вышерасположенными центрами иннервации проекционно, а также с помощью нейрогуморальных и рефлекторных механизмов [5]. Однако следует отметить, что концепции регуляции функции нижних мочевых путей в норме и патологии являются в большей степени эмпирическими, и единого понимания этого вопроса на сегодняшний день нет.
Клиническая картина
Врачу-неврологу, курирующему пациента с осложненной травмой позвоночника, необходимо оценить уровень и степень повреждения спинного мозга и учесть посттравматические сроки. Клиническая картина в острый и ранний периоды после получения травмы обусловлена спинальным шоком, что проявляется арефлексией и задержкой мочи. По мере восстановления можно наблюдать активизацию рефлекторной деятельности и формирование «в сухом остатке» нейрогенного расстройства мочеиспускания. При повреждении спинного мозга на уровне сакрального центра мочеиспускания и периферических нервных волокон развивается атония или гипотония детрузора, при этом за счет интактности симпатических структур иннервации внутренний уретральный сфинктер сохраняет сократительную способность. Таким образом, нарушается взаимосвязь симпатических и парасимпатических влияний [6]. Клинически наблюдается нейрогенная задержка мочеиспускания с элементами парадоксальной ишурии (выделения мочи по каплям на фоне переполненного мочевого пузыря). При локализации травмы выше сакрального центра и ядра Онуфа повреждаются проводниковые нервные волокна, осуществляющие взаимосвязь регулирующих структур, однако сами центры иннервации могут быть интактны. В этом случае и детрузор, и внутренний сфинктер уретры способны к циклическому сокращению и расслаблению, но рассогласованность в работе приводит не к нормальному акту мочеиспускания, а к детрузорно-сфинктерной диссинергии. Поражение на уровне нижнегрудного и верхнепоясничного отделов позвоночника, вовлекающее симпатические регулирующие структуры, вызывает нарушение сократительной способности внутреннего сфинктера уретры и недержание мочи. Травма спинного мозга на уровне шейного и верхнегрудного отделов позвоночника ведет к прерыванию взаимосвязи спинальных и стволовых, а также кортикальных структур регуляции. В ситуации, когда центры иннервации спинного мозга и нервные проводники между ними сохраняют свою анатомическую целостность, клинически может сформироваться автономный процесс мочеиспускания, а также гиперактивность мочевого пузыря. В этом случае накопление и выделение мочи происходят рефлекторно, в т. ч. с участием аксон-рефлексов, без контроля центров, отвечающих за произвольную составляющую физиологического процесса [7].
Описанные клинические нарушения достаточно вариабельны и зависят от характера и тяжести повреждения, а также сроков, прошедших с момента травмы, поэтому можно наблюдать переход одной формы нейрогенного расстройства мочеиспускания в другую.
Невролог, понимая обусловленность клинической картины уровнем поражения спинного мозга, определяет тактику ведения спинального пациента и дальнейший прогноз. Осуществление адекватной коррекции урологических осложнений лежит, несомненно, в междисциплинарной плоскости. В связи с этим нейроурологическая практика, а вернее, четкое и скоординированное взаимодействие невролога и уролога способно обеспечить квалифицированную и своевременную помощь. И если врач-невролог сосредоточен на повреждении спинного мозга и нарушении иннервации, то уролог контролирует непосредственное функциональное состояние нижних мочевых путей и коррекцию сопутствующих воспалительных и нефротических осложнений. Отсюда вытекает необходимость тесной взаимосвязи специалистов для полноценной коррекции нейрогенных расстройств мочеиспускания.
В представлении уролога, оказывающего специализированную помощь пациентам с неврологическими расстройствами, процесс мочеиспускания выглядит несколько сложнее, чем простой циклический акт, состоящий из чередования фаз накопления и выведения мочи, обеспеченный двумя основными функциями мочевого пузыря: резервуарной и эвакуаторной. Функционально этот процесс определяется синергией детрузора с гладкомышечным сфинктером уретры и мышцами тазового дна, включающими наружный уретральный сфинктер.
Физиологически мочевой пузырь, природой созданный резервуар для сбора мочи, обладает способностью к полному опорожнению в подходящее время и в удобном для совершения акта мочеиспускания месте согласно социально-поведенческим нормам. Эта крайне важная способность реализуется в результате сложной регуляции с участием центральной и периферической нервных систем. Фундаментально акт мочеиспускания – это спинальный рефлекс, обеспечиваемый работой центров головного мозга, реализация и подавление этого рефлекса находятся под волевым контролем. Возможность произвольного управления делает функцию нижних мочевых путей уникальной по сравнению, например, с сердечно-сосудистой системой, и в то же время более уязвимой при неврологических заболеваниях [8]. Таким образом, основными функциями нижних мочевых путей являются накопление мочи в мочевом пузыре, длящееся относительно продолжительное время, и мочеиспускание, занимающее в норме несколько секунд. Реципрокные отношения – расслабление/напряжение детрузора, закрытие уретрального сфинктера и сокращение/расслабление детрузора, открытие уретрального сфинктера – обеспечивают скоординированность процессов накопления и удаления мочи и находятся под нейромедиаторным контролем [9].
Нейрогенная дисфункция нижних мочевых путей является следствием патологии центральной нервной системы или периферических нервных окончаний ‒ отделов нервной системы, выполняющих контроль над актом мочеиспускания. В этом состоит главное отличие рассматриваемого нарушения от нарушений нижних мочевых путей ненейрогенной этиологии, развивающихся вследствие поражения непосредственно мочеполовой системы.
В урологическом сообществе длительное время основной опорой для определения формы нейрогенного расстройства мочеиспускания являлась классификация, предложенная профессором Г. Мадерсбахером в 1980 г. и рекомендуемая Европейской ассоциацией урологов (рис. 1) [10]. В ней автор выделяет 8 основных форм нейрогенных расстройств мочеиспускания в зависимости от состояния детрузора и внутреннего сфинктера уретры. Подразумевается, что указанные структуры могут быть в гипертонусе, гипотонусе и в нормальном состоянии. Однако сложность в постановке диагноза и категоричность в выборе одной из 8 форм нарушений мочеиспускания сегодня заставляют говорить о пересмотре форм расстройств мочеиспускания. С клинической точки зрения все возможные виды нарушений мочеиспускания рассмотреть в рамках одной из существующих классификаций невозможно. В определении поражения у пациента наиболее часто специалисты основываются на преобладающем нарушении эвакуаторной или резервуарной функции мочевого пузыря, различных видах детрузорно-сфинктерной диссинергии и уродинамических показателях максимального детрузорного давления в точке утечки. При этом важность знания о максимальном детрузорном давлении и максимальном давлении в точке утечки делает необходимым проведение специализированного уродинамического исследования практически каждому пациенту с нарушениями мочеиспускания на фоне неврологического заболевания.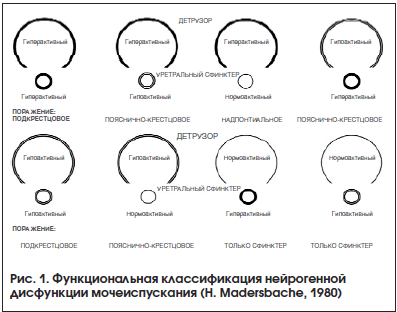
Лечение
Основными задачами урологической помощи на всех этапах нейрореабилитации являются:
1) сохранение и обеспечение функции верхних мочевыводящих путей;
2) независимость регуляции функции нижних мочевыводящих путей;
3) улучшение качества жизни.
С практической точки зрения важны борьба с вторичными осложнениями нейрогенной дисфункции мочеиспускания, а также их профилактика. К таким осложнениям относятся манифестация инфекции мочевыводящих путей (исключая бессимптомную бактериурию), уролитиаз, микроцистис, гидронефротическая трансформация и почечная недостаточность, стриктура уретры и т. д. [11].
Наименьшего риска осложнений со стороны верхних мочевыводящих путей следует ожидать при сохранении резервуарной функции мочевого пузыря с низким внутрипузырным давлением, например при гипотонии детрузора, его достаточной функциональной емкости и нормальном состоянии поперечно-полосатого сфинктера уретры или его гипотонии. В этом случае к хорошим результатам коррекции, в т. ч. улучшению качества жизни спинального пациента, приводит адекватное дренирование нижних мочевых путей, при этом следует руководствоваться международными стандартами и отечественными клиническими рекомендациями. При нарушении функции опорожнения мочевого пузыря вследствие повреждения позвоночника и спинного мозга методом выбора является асептическая периодическая катетеризация. Она подразумевает использование одноразового стерильного лубрицированного катетера. Процедура выполняется самостоятельно или с посторонней помощью каждые 4‒6 ч [12].
Иные методы дренирования мочевого пузыря, такие как приемы Креде или Вальсальвы, длительное использование постоянного мочевого катетера, должны быть строго обоснованы, т. к. несут значительные риски развития вторичных нейрогенных осложнений работы мочевого пузыря, достигающих 34% [13].
Периодическая катетеризация 4‒6 раз в сутки при условии отсутствия выраженных нарушений со стороны верхних мочевыводящих путей, шокового состояния, гнойно-инфекционных процессов в уретре и мочевом пузыре может быть назначена любым специалистом, курирующим пациента. Вопрос о том, когда переводить пациента на периодическую катетеризацию для постоянного уретрального дренажа, находится в стадии обсуждения сообщества специалистов по нейроурологии [14]. Формальных ограничений и четких рекомендаций по срокам нет, однако считается, что при отсутствии противопоказаний и достаточной укомплектованности отделения средним и младшим медицинским персоналом следует избавлять пациента от постоянных дренажей как можно раньше.
Гиперактивный мочевой пузырь, встречающийся на фоне детрузорно-сфинктерной диссинергии и без нее, является другой формой нейрогенного расстройства мочеиспускания вследствие травмы позвоночника и спинного мозга. Если такой тип нарушения клинически проявляется недержанием мочи, то он не несет значительного риска осложнений со стороны верхних мочевыводящих путей. К проблемам нейрогенного гиперактивного мочевого пузыря следует отнести снижение качества жизни.
Детрузорно-сфинктерная диссинергия характеризуется тем, что в момент напряжения мочевого пузыря для его опорожнения происходят различные по силе и продолжительности сокращения внутреннего и наружного сфинктеров уретры, обеспечивающих функцию удержания. В норме сокращения детрузора синхронны с расслаблением этих сфинктеров, что способствует свободному выведению мочи по уретре. Нарушение функции опорожнения в сочетании с высоким внутрипузырным давлением ‒ наиболее опасная форма нейрогенной дисфункции мочеиспускания из-за развития пузырно-мочеточникового рефлюкса, а также возможности структурных повреждений самого мочевого пузыря. В этом случае перед урологом стоят две основные задачи: 1) подавление высокого внутрипузырного давления, 2) обеспечение оттока мочи по уретре.
Для подавления детрузорной гиперактивности в качестве первой линии терапии применяются антихолинергические средства, в дополнение к которым можно назначать препараты из группы бета-3-адреномиметиков [15]. Вторая линия лечения включает инъекционное введение в стенку мочевого пузыря 200 ЕД ботулинического нейропептида. Надо понимать, что терапия направлена на создание низкого внутрипузырного давления в мочевом пузыре, необходимого для нормальной работы верхних мочевых путей. Одним из результатов купирования гиперактивности, особенно при сохранении нормального или повышенного тонуса поперечно-полосатого сфинктера уретры, будет увеличение количества остаточной мочи или отсутствие мочевыделения. Поэтому крайне важно объяснить пациенту необходимость проведения указанной терапии с назначением периодической катетеризации мочевого пузыря.
При своевременной коррекции нарушений мочеиспускания у спинальных пациентов, применении рекомендованного метода отведения мочи, компенсации избыточного внутрипузырного давления вследствие гиперактивности детрузора или детрузорно-сфинктерной диссинергии удается избежать многих вторичных осложнений.
В комплексной программе реабилитационного лечения пациентов с травмой позвоночника и спинного мозга используются методики немедикаментозной коррекции, показавшие различный терапевтический потенциал в ходе исследований. В частности, применение электростимуляции мочевого пузыря с помощью имплантируемых электродов в работе А.В. Лившица и соавт. показало, что создать управляемый акт мочеиспускания невозможно, т. к. возбуждение детрузора распространяется на внутренний сфинктер уретры, моделируя детрузорно-сфинктерную диссинергию [16]. Несмотря на то что исследователи представили некоторые положительные результаты, методика не нашла клинического применения в связи с высокой инвазивностью и риском вторичных осложнений.
Применение электростимуляции переменным пульсирующим током по лонно-сакральной методике и электрофореза с прозерином на передней брюшной стенке в проекции мочевого пузыря в настоящий момент представляется несостоятельным вследствие особенностей физиологии нижних мочевых путей и неучастия мышц живота в акте мочеиспускания.
Перспективно использование современных методик: сакральной инвазивной электронейростимуляции с помощью имплантируемых электродов и ритмической периферической магнитной стимуляции в области сакрального центра мочеиспускания и крестцовых корешков [17, 18]. В настоящее время механизм действия магнитной стимуляции на физиологию нижних мочевых путей остается неясным. Многоступенчатость и сложность нервной регуляции процесса удержания мочи и акта мочеиспускания предполагают возможность вовлечения различных структур в ответ на внешнее воздействие. Клинические и уродинамические эффекты магнитной стимуляции, вероятно, связаны с восстановлением интеграции регуляторных рефлексов, при этом наблюдается эффект нейромодуляции, когда происходит изменение активности (торможение или возбуждение) структур центральной, периферической и вегетативной нервных систем [19, 20].
Нейрогенное нарушение мочеиспускания, обусловленное травмой позвоночника и спинного мозга, клинически чрезвычайно гетерогенно вследствие вариабельности уровня и степени тяжести поражения [21, 22]. Этот аспект диктует необходимость индивидуального диагностического подхода, выбора адекватного метода коррекции работы нижних мочевых путей. Реабилитационный путь спинального пациента в настоящее время невозможно представить без тесного сотрудничества невролога и уролога. Совместный современный подход специалистов к проблеме урологических осложнений травмы спинного мозга обеспечивает пациенту верное понимание собственного состояния и адекватную прогностическую оценку, а также возможность социальной адаптации и повышения качества жизни [23, 24].
Источник

Межпозвоночная грыжа — распространенное заболевание опорно-двигательного аппарата, при котором фрагменты межпозвоночного диска выпячиваются или выпадают в позвоночный канал. Коварство заболевания в том, что на начальной стадии оно почти не беспокоит пациента, но без лечения и соблюдения осторожности патология быстро прогрессирует.
Патология нередко вызывает болезненные симптомы, на первый взгляд не связанные с позвоночником. Межпозвонковая грыжа может привести к параличу, вызвать нарушения мочеиспускания и дефекации, спровоцировать скачки артериального давления.
Как развивается заболевание
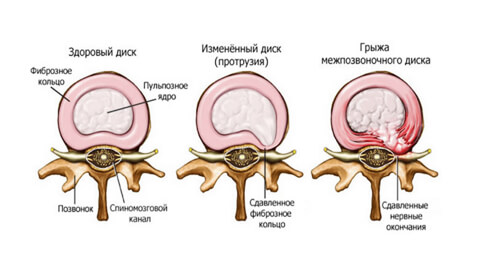
Молодой здоровый позвоночник подвижен и эластичен. Каждые позвоночный диск имеет оболочку — фиброзное кольцо. Внутри него заключено пульпозное ядро — студенистый хрящевидный наполнитель.
При травмах, чрезмерных нагрузках, заболеваниях, нарушении обмена веществ в фиброзном кольце появляются трещины или разрывы. Некоторое время пульпозное ядро удерживается продольной связкой, но потом выходит наружу — полностью или частично.

Есть четыре стадии развития болезни:
- Пролапс. При этой стадии небольшой фрагмент пульпозного ядра (до 3 мм) выходит за пределы диска, не нарушая его оболочку. Причина — первые дегенеративные изменения, нарушение кровоснабжения, обезвоживание, растрескивание оболочки.
Симптомы протрузии похожи на проявления остеохондроза: после физических нагрузок пациента беспокоит ноющая боль, он быстро утомляется. На этой стадии пациенты редко обращаются за врачебной помощью, списывая происходящее на усталость или возраст.
- Протрузия. От 4 до 16 мм пульпозного ядра выходит за пределы анатомических размеров фиброзного кольца. Это нарушает кровоснабжение диска, ядро давит на фиброзную оболочку и вызывает боль. Но если не зажаты кровеносные сосуды и нервы, она не слишком интенсивна.
На этой стадии оболочка диска еще не повреждена, но игнорировать симптомы уже опасно. Ведь если пациенту повезло меньше и выпятившееся ядро все же сдавило нерв, он будет страдать от нарушения чувствительности рук и ног, онемения и холода в пальцах. Если протрузия произошла в шейном отделе, может подниматься артериальное давление, начаться мигрень, головокружения, упасть зрение. Если в поясничном отделе — возникает люмбалгия и нарушения в работе органов малого таза.
- Экструзия. Ядро «выдавлено» со своего места на 6-15 мм, то есть почти полностью, но его форма сохранена. Человек ощущает резкую боль, ограничение подвижности, мышцы каменеют, возникает отек мягких тканей. «Прострел » происходит при каком-то внешнем воздействии: при поднятии тяжестей, резком движении, травме, простуде или стрессе.
На этом этапе хирургическое вмешательство не понадобится. Достаточно медикаментозно снять болевой синдром, отек и спазм мышц. Когда ослабеет спазм нервных окончаний, врач составит индивидуальную программу реабилитации. Это позволит избежать рецидивов.
- Секвестрация. Ядро выпадает, межпозвонковый диск защемляет нервные окончания, боль становится постоянной. Выпячивание ущемлено, питание тканей невозможно и оно отмирает, вызывая воспаление. В самом сложном случае грыжа выдавливается в спинномозговой канал и там провоцирует гнойные процессы.
Кроме сильной боли и скованности секвестированная грыжа может вызвать неврологические болезни, отказ работы внутренних органов, лишить способности двигаться самостоятельно. В этом случае промедление опасно, его последствия могут быть необратимы. Если безоперационная терапия неэффективна, врач предложит хирургическое вмешательство.
Какие бывают межпозвоночные грыжи
Болезнь имеет градацию по нескольким признакам.
По расположению:
- в поясничном отделе. Самый распространенный тип патологии, до 65 % грыж возникают именно в пояснице;
- в грудном отделе, до 31% случаев;
- в области шеи, 4%.
По времени возникновения:
- Первичные;
- Вторичные, возникают вследствии дегенерации диска.
По анатомическим особенностям:
- свободная. Продольная связка сохраняет вертикальное положение позвоночника, содержимое пульпозного ядра проходит через нее.
- блуждающая. Ядро вытекает, отрывается от диска и перемещается по спинномозговому каналу;
- Перемещающаяся. Возникает при травме или экстремальной нагрузке, сопровождающейся смещением диска. Когда нагрузка исчезает, ядро может вернуться на место или закрепиться в неправильной позиции.
По направлению выпадения ядра:
- Переднебоковая, находится в передней части позвонка. Внедряется в продольную связку и вызывает сильную боль.
- Заднебоковая, проникает сквозь заднюю стенку фиброзного кольца
По виду тканей, которые выступают за границы кольца:
- пульпозная, возникает когда ядро выдавливается через трещины фиброзного кольца;
- хрящевая, в этом случае выдавливается потерявший эластичность хрящ;
- костная, на нервные окончания давят костные разрастания и остеофиты. Чаще встречается у пожилых пациентов, страдающих спондилёзом.
Важно! у пациента одновременно могут возникнуть несколько разных видов межпозвонковых грыж. Необходимо внимательно исследовать каждый болезненный участок и дифференцировать лечение.
Причины возникновения и факторы риска
Определить этиологию болезни в каждом конкретном случае непросто, ведь пусковым механизмом может стать несколько причин или хронические заболевания. Самыми распространенными являются:
- травмы позвоночника;
- наследственная предрасположенность;
- доброкачественные или злокачественные новообразования;
- болезни позвоночника — лордоз, сколиоз, остеохондроз;
- инфекционные и вирусные заболевания;
- лишний вес;
- тяжелые физические нагрузки;
- беременность;
- малоподвижный образ жизни;
- возрастные изменения.
Симптомы грыжи позвоночника
Небольшие грыжи межпозвоночного диска не давят на нервные окончания и пациент не подозревает о заболевании. Первые проявления легко перепутать с признаками остеохондроза. Но чем сильнее разрушается фиброзное кольцо, тем интенсивнее становятся боль. Кроме того, первыми признаками грыжи являются:
- отечность и напряженность мышц;
- кифоз или сколиоз;
- ощущение жжения, покалывания;

Боли при грыже могут быть тупыми ноющими и острыми, рвущими или стреляющими. Пациент ищет положение, в котором страдания ослабевают и принимает вынужденное положение, рефлекторно изгибая позвоночник. Нарушается походка, болезненны не только мышцы поясницы, ягодиц и голени, но даже кожа. В ответ на легкий укол или щипок она проявляет гиперестезию — резкую болезненность. Меняются рефлексы коленных или ахилловых сухожилий. Появляется слабость и легкая атрофия ног, дряблость мышц.
При грыже пациент ощущает боли постоянно. Они усиливаются при определенных движениях, ходьбе, кашле, чихании, иногда сопровождаются повышением температуры, онемением рук и ног.
Дополнительные симптомы зависят от локализации грыжи. Если патология развивается в шейном отделе— это головная боль и зажатость шеи, тошнота, шум в ушах повышение внутричерепного давления и даже эпилепсия.
При повреждении грудного отдела боль имитирует сердечный приступ, в пояснице — простреливает в бедро. Нередко поясничная грыжа вызывает частое и болезненное мочеиспускание, обострение геморроя, непривычную потливость или сухость ног.
Чем опасно заболевание
Если пациент не находит времени на полноценное лечение, он серьезно рискует собственным здоровьем. Самая серьезная опасность — полный паралич, он возникает вследствии выраженного пролапса, когда деформированный хрящ повреждает спинной мозг.
Грыжа поясничного отдела позвоночника приводит к нарушению иннервации органов брюшной полости и малого таза: дисфункции кишечника, мочевого пузыря, репродуктивных органов, снижению мышечной силы, ущемлению седалищного нерва. У мужчины развивается аденома простаты. Геморрой и варикозное расширение вен — тоже следствие нарушений в работе опорно-двигательного аппарата.
Грыжа грудного отдела вызывает коксартроз, нарушает правильное положение структур коленного сустава, постановку стоп. Искривляется положение берцовых костей.
Увеличивающаяся грыжа шейного отдела может спровоцировать ишемический инсульт, сопровождающийся парализацией, утратой речи, атаксией. В области шеи расположены важнейшие кровеносные сосуды, нарушение их проходимости повлечет проблемы мозгового кровообращения. Следствием будут парезы, боль в локтевых суставах, запястьях и плечах, нарушения в работе легких, сердца и щитовидной железы.
Диагностика
Врачебную помощь при заболевании оказывают невролог, терапевт и ортопед. Первые тревожные сигналы врач заметит при визуальном осмотре пациента — нарушение осанки и недостаточную чувствительность участков тела в зоне действия защемленного нерва. Прощупывая позвоночник специалист определит, насколько спазмированы и болезненны мышцы и местоположение патологии. Вас могут попросить согнуться и разогнуться, чтобы оценить ограничение подвижности. Врач проведет диагностику рефлексов в коленном и ахилловом сухожилии.
Размер и локализацию грыжи поможет определить МРТ, КТ и рентгенография в боковой и фронтальной проекциях.
Методы лечения
Первостепенная задача — облегчить состояние пациента, поэтому терапия начинается с приема обезболивающих средств и полного покоя. Для устранения болевых неврологических проявлений врач выпишет противовоспалительные нестероидные препараты, миорелаксанты, лечебные мази — раздражающего действия и для снятия отечности.
Надежный способ обезболивания пораженного участка — рентген-контролируемая блокада. Под местным обезболиванием врач введёт лекарство в место пережима нервных окончаний.
Когда появится устойчивая положительная динамика, врач скорректирует прием лекарств. Главное на этом этапе — следовать комплексу лечебно-профилактических мероприятий. За динамикой лечения будет наблюдать невропатолог, пациент должен проходить осмотр не реже, чем раз в месяц.
Для восстановления хрящевой ткани применяются хондропротекторы. Минимальный курс лечения — 3 месяца. Хорошо зарекомендовали себя препараты для улучшения кровообращения. Важно провести курсовой прием витаминов группы В, D, A, E. Это улучшит питание тканей и запустит процессы восстановления.
При лечении грыжи к хирургическому вмешательству прибегают только в крайних случаях: при большом размере грыжи и ее секвестрации, если нарушены важнейшие жизненные процессы или консервативная терапия оказалась неэффективной.
Безоперационные методы лечения
После полного обследования врач может рекомендовать лечение грыжи позвоночника средствами мануальной или физиотерапии. Однако эти методы оправданы только в отношении небольших грыж безопасной локализации.
Самые популярные методы безоперационного лечения:
- гирудотерапия. Фермент слюны пиявок способствует рассасыванию грыжи и улучшает кровообращение;
- криотерапия. При действии жидкого азота в пораженном участке активнее циркулирует кровь, благодаря чему улучшается питание тканей;
- остеопатия. Специалист активирует обменные процессы в тканях организма, снимая блоки, зажимы и застойные процессы при помощи массажа и точечного воздействия;
- иглоукалывание. Воздействие на организм пациента при помощи безболезненных направленных проколов специальными иглами.
Лучшими средствами физиотерапии грыжи позвоночника являются:
- массаж;
- лечебная физкультура;
- УВЧ;
- электрофорез и фонофорез;
- рефлексотерапия.
Каждый метод имеет свои особенности и противопоказания, оптимальный комплекс порекомендует лечащий врач.
Мануальная терапия не исцеляет заболевание, она лишь на некоторое время облегчает самочувствие пациента. Главное, что должен сделать пациент — исключить факторы риска и заботится о состоянии позвоночника.
Физические нагрузки
Отказываться от посильных физических упражнений нельзя. Разумные нагрузки мягко разгоняют застойные процессы, мышечный корсет обеспечивают стабильность грыжи. Движение восстанавливает правильный двигательный стереотип и симметрию движения.
Однако есть упражнения, которые категорически запрещены при грыже позвоночника:
- движения, связанные с осевой нагрузкой на позвоночник — поднятие гантелей, штанги, перенос тяжестей, жим ногами и скручивания;
- физическая активность, сопровождающаяся длительным пребыванием в вертикальном положении — бег, футбол, катание на лыжах.
- упражнения на прямых ногах и связанные с сокращением мышц спины;
- глубокие приседания.
Под запретом игра в гольф, бодибилдинг и конный спорт.
Занимайтесь плаванием, аквааэробикой, йогой и пилатесом, выполняйте разработанный тренером комплекс ЛФК. Полезна скандинавская ходьба, ведь в этом случае нагрузка распределяется и на спортинвентарь.
Профилактика
Чтобы не допустить опасного заболевания, необходимо:
- Улучшить подвижность позвоночника;
- Нормализовать питание диска;
- Сформировать мышечный корсет.
Это комплексный подход, он требует настойчивости и изменения образа жизни.
Чтобы свести опасность к минимуму:
- нормализуйте вес. Избыточная масса тела — это тяжелое испытание для позвоночника и всего опорно-двигательного аппарата. Но сбрасывайте килограммы постепенно, одновременно укрепляя мышечный корсет;
- следите за осанкой. Так нагрузка будет равномерно распределятся на каждый отдел позвоночника, это исключит застойные процессы, отеки и спазмы;
- откажитесь от курения. Циркулирующий в крови никотин затрудняет питание межпозвоночного диска, хрящевые ткани сохнут и растрескиваются;
- проходите сеансы массажа. Это улучшит кровообращение в малоподвижных зонах позвоночника, поддержит в тонусе мышцы и межпозвоночные диски;
- питайтесь сбалансированно. Продукты должны полностью восполнять потребность в витаминах, микроэлементах, жирах. Тяжелую балластную пищу следует исключить. Для здоровья позвоночника полезен животный белок, овощи и фрукты без термической обработки.
- не перегружайте спину, выполняйте разминку перед комплексом упражнений;
- прыгая, не приземляйтесь на пятки;
- отработайте технику бега, исключив сотрясения и жесткую постановку стопы;
- не сидите в одном положении более 30 минут;
- не сутультесь, следите за постановкой головы;
- не спите на мягком матрасе.
Источник
