Грыжа морганьи справа кто

Лучевая диагностика грыжи Морганьиа) Терминология: б) Визуализация грыжи Морганьи: • Рентгенография: • КТ и МРТ:
в) Дифференциальная диагностика: г) Клинические особенности: – Вернуться в оглавление раздела “Лучевая медицина” Редактор: Искандер Милевски. Дата публикации: 23.1.2020 |
Источник
Анатомической основой парастернальной диафрагмальной грыжи, или грыжи Морганьи (ГМ), является дефект развития диафрагмы с образованием «слабой» зоны в области грудинореберного треугольника, лишенной мышечных волокон [1, 3, 9, 25]. Частота ГМ составляет 1 на 1 млн населения. Тематические публикации немногочисленны и основаны на небольшом количестве наблюдений [5, 7, 8, 34]. Еще более редко встречается сочетание ГМ с хирургическими заболеваниями сердца [10, 19, 21, 29]. Представлено наблюдение левосторонней ГМ в сочетании с послеоперационной вентральной грыжей, дефектом и аневризмой межпредсердной перегородки и аномальным впадением венозного коллектора из поперечной ободочной кишки в правое предсердие.
Больная А., 55 лет, поступила с жалобами на одышку, тянущие боли за грудиной, тяжесть в эпигастральной области и отрыжку после приема пищи. Росла и развивалась нормально.
В возрасте 35 лет был выявлен порок сердца – дефект межпредсердной перегородки без клинических проявлений. Перечисленные жалобы появились в 2010 г. По месту жительства сначала была заподозрена релаксация левого купола диафрагмы, а затем – грыжа пищеводного отверстия диафрагмы. Только при КТ, проведенной в федеральной клинике, заподозрена ГМ. Несмотря на большие размеры грыжи и наличие жалоб, от хирургического вмешательства воздержались в связи с имеющимся дефектом межпредсердной перегородки. В 1991 г. больной выполнили пластику брюшной стенки местными тканями по поводу пупочной грыжи. Через год наступил ее рецидив.
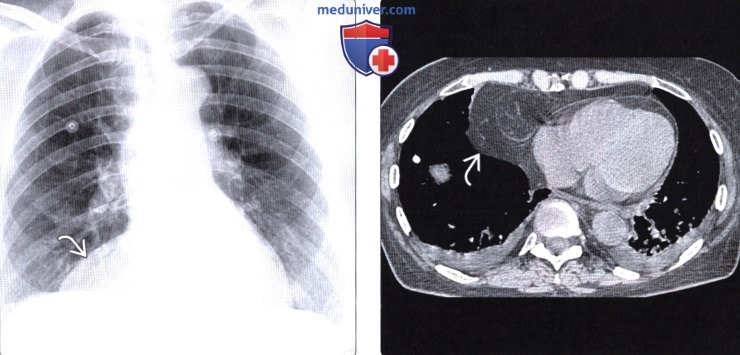
При поступлении состояние удовлетворительное. В легких дыхание везикулярное, ослаблено слева в нижних отделах. Тоны сердца приглушены. Во втором межреберье слева от грудины систолический шум средней интенсивности. В области срединного послеоперационного рубца передней брюшной стенки определяется грыжевое выпячивание размером 6×6 см, содержимое которого свободно вправляется в брюшную полость. Печень не увеличена. Периферических отеков нет. ЭКГ: синусовая брадикардия, отклонение электрической оси сердца вправо, гипертрофия правого желудочка. ЭхоКГ: лоцируется аневризма межпредсердной перегородки размером 17×27 мм, где при допплерографии отмечен сброс крови слева направо. Чреспищеводная ЭхоКГ: фестончатая аневризма межпредсердной перегородки с множественными дефектами от 2 до 8 мм в диаметре. МСКТ (рис. 1): Рисунок 1. Мультиспиральная компьютерная томограмма. Грыжа Морганьи. в левой половине грудной клетки ретростернально, прилегая к передней грудной стенке, оттесняя левое легкое краниально, а сердце дорсально, визуализируется сегмент толстой кишки, окруженный жировой тканью (сальник и брыжейка толстой кишки). В передних отделах диафрагмы определяется дефект размером 5,1×9,0 см. Сердце увеличено за счет правых отделов. В центральной части межпредсердной перегородки визуализируется аневризма размером 16×27 мм со сбросом крови слева направо через отверстия в аневризме (рис. 2).
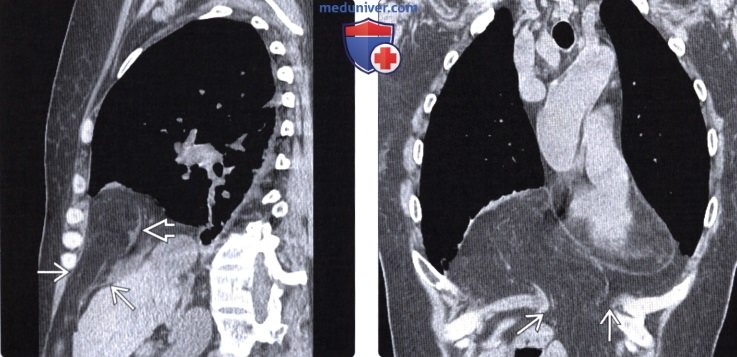
Рисунок 1. Мультиспиральная компьютерная томограмма. Грыжа Морганьи. в левой половине грудной клетки ретростернально, прилегая к передней грудной стенке, оттесняя левое легкое краниально, а сердце дорсально, визуализируется сегмент толстой кишки, окруженный жировой тканью (сальник и брыжейка толстой кишки). В передних отделах диафрагмы определяется дефект размером 5,1×9,0 см. Сердце увеличено за счет правых отделов. В центральной части межпредсердной перегородки визуализируется аневризма размером 16×27 мм со сбросом крови слева направо через отверстия в аневризме (рис. 2). Рисунок 2. Мультиспиральная компьютерная томограмма сердца. Аксиальный срез: в центральной части межпредсердной перегородки визуализируется аневризма (стрелки) размером 16×27 мм со сбросом крови слева направо через отверстия в аневризме (по данным серии срезов). В правое предсердие впадает венозный ствол диаметром до 8 мм, отходящий от сегмента толстой кишки, расположенного в грыжевом мешке (рис. 3).
Рисунок 2. Мультиспиральная компьютерная томограмма сердца. Аксиальный срез: в центральной части межпредсердной перегородки визуализируется аневризма (стрелки) размером 16×27 мм со сбросом крови слева направо через отверстия в аневризме (по данным серии срезов). В правое предсердие впадает венозный ствол диаметром до 8 мм, отходящий от сегмента толстой кишки, расположенного в грыжевом мешке (рис. 3). Рисунок 3. Мультиспиральная компьютерная томограмма сердца. а – объемные реконструкции сердца.
Рисунок 3. Мультиспиральная компьютерная томограмма сердца. а – объемные реконструкции сердца. Рисунок 3. Мультиспиральная компьютерная томограмма сердца. б – объемные реконструкции сердца.
Рисунок 3. Мультиспиральная компьютерная томограмма сердца. б – объемные реконструкции сердца. Рисунок 3. Мультиспиральная компьютерная томограмма сердца. в – MIP-реконструкция: в правое предсердие впадает венозный ствол, отходящий от толстой кишки, расположенной в грыжевом мешке.
Рисунок 3. Мультиспиральная компьютерная томограмма сердца. в – MIP-реконструкция: в правое предсердие впадает венозный ствол, отходящий от толстой кишки, расположенной в грыжевом мешке.
Поставлен диагноз: врожденный порок сердца, аневризма межпредсердной перегородки с множественными дефектами. Диафрагмальная ГМ. Рецидивная вентральная грыжа. Аномальный венозный сосуд брыжейки толстой кишки, впадающий в правое предсердие.
01.09.11 больная оперирована. Верхнесрединная лапаротомия. В области левого реберно-грудинного треугольника выявлен дефект овальной формы размером 10×5 см, через который в переднее средостение проникает поперечная ободочная кишка с большим сальником. Грыжевое содержимое плотно фиксировано в области ворот множественными спайками. После адгезиолизиса сальник резецирован, петля кишки низведена в брюшную полость. Выполнена срединная стернотомия. Грыжевой мешок, расположенный на передней поверхности перикарда, резецирован. Полость перикарда запаяна. Сердце частично выделено из сращений. При этом между диафрагмой и правым предсердием выявлено мышечное сращение диаметром до 1,5 см, содержащее аномальный венозный сосуд. Подключен аппарат искусственного кровообращения. Разрез стенки правого предсердия. В области овальной ямки аневризма межпредсердной перегородки с дефектами от 2 до 9 мм. Аневризма иссечена и произведена пластика аутоперикардом. Кардиохирургический этап завершен послойным ушиванием стернотомического разреза с фиксацией распила грудины 4 скобами из никелида титана. Лоскут левого купола диафрагмы подшит к реберной дуге и реберно-грудинному сочленению отдельными П-образными швами лавсаном. На всем протяжении лапаротомной раны, включая область грыжевых ворот, мобилизованы края апоневроза шириной 5 см и ушиты край в край. Линия первичного шва укреплена полипропиленовым сетчатым эндопротезом размером 30×10 см по типу on lay, который по периметру фиксирован обвивным швом. Послойное ушивание раны.
Послеоперационный период протекал удовлетворительно. Операционная рана зажила первичным натяжением. Пациентка обследована через 1 год после операции. Рецидива грыжи нет. Внутрисердечного сброса крови нет, правые полости сердца уменьшились в размерах.
В 1761 г. G. Morgagni опубликовал наблюдение выявленной на аутопсии грыжи с выходом содержимого брюшной полости в грудную через правую грудинореберную щель [37]. D. Larrey в 1824 г. осуществил хирургический доступ в полость перикарда через дефект в области левого стернокостального треугольника диафрагмы. Грыжи этой области получили название Морганьи или Ларрея (как ретростернальные, так и ретрокостостернальные) и, согласно отечественной традиции, объединены в группу истинных парастернальных грыж слабых зон диафрагмы [4, 7].
ГМ – редкое заболевание, его доля составляет от 2 до 6% всех грыж диафрагмы [16, 25, 28]. Возможна их комбинация с другими видами диафрагмальных грыж [15]. ГМ может быть врожденной [1, 30], однако от 80 до 100% таких грыж имеют хорошо сформированный грыжевой мешок (брюшина и плевра) и являются приобретенными [5, 7, 13, 25].
Тематическая литература преимущественно второй половины XX века содержит относительно небольшое число наблюдений [7, 34]. Л.Д. Линденбратен [4] приводит описание 23, Б.В. Петровский и соавт. [7] – 9, К.Т. Овнатанян и Л. Г. Завгородний [6] – 10, И.Х. Рабкин и А.А Акпербеков [8] – 11, С.М. Луценко [5] – 9 наблюдений. В отечественной литературе к 1966 г. имелось 60 описаний этой разновидности диафрагмальных грыж [7].
T. Comer и O. Clagett [13] представили опыт лечения 50 больных в разных клиниках. Современные авторы P. Minneci и соавт. [25] за 15-летний период наблюдали 12 больных, Y. Karamustafaoglu и соавт. [20] за 10 лет – 13 больных.
Мнения о возрастном составе больных ГМ противоречивы. Так, J. Barut и соавт. [11], S. Dutta, C. Albanese [14] сообщают о преимущественной диагностике ГМ в детском возрасте. По другим данным, возраст больных был от 30 до 65 лет [7, 8, 25]. ГМ чаще встречается у женщин (от 70 до 90%) [13, 20].
В представленном нами наблюдении ГМ клинически проявилась у женщины старше 50 лет и имела хорошо выраженный грыжевой мешок, что свидетельствовало о приобретенном характере заболевания. По-видимому, у этой больной имеется врожденный дефект соединительной ткани, что подтверждает пупочная грыжа в анамнезе с ее рецидивом после пластики местными тканями и аневризма межпредсердной перегородки с множественными отверстиями.
Преимущественная локализация ГМ в области правого грудинореберного треугольника [4, 8, 13, 25, 27]. Некоторые авторы наблюдали и двустороннюю парастернальную грыжу [1, 4, 6, 13, 19]. В нашем наблюдении была редкая левосторонняя локализация грыжи. Наиболее часто содержимым грыжи является большой сальник и поперечная ободочная кишка [7, 8, 12], реже – желудок (до 12%), еще реже – селезенка, почка, надпочечник или содержимого может не быть [13, 17, 25].
Заболевание чаще протекает бессимптомно и является случайной находкой [4, 7, 23]. Симптомы, обусловленные обструкцией или сдавлением дислоцированных органов брюшной полости или компрессией легкого, отмечают у 28-50% больных [13, 20, 25]. Тогда заболевание проявляется одышкой, изжогой, периодической тошнотой и рвотой, вздутием живота [7, 26]. Первым проявлением ГМ может стать недостаточность кровообращения по большому кругу, легочная гипертензия вследствие сдавления легкого и даже сердечная тампонада [24, 32, 36].
Провоцирует возникновение ГМ высокое интраабдоминальное давление вследствие травмы, беременности или ожирения [34]. Отмечено, что у тучных больных доминируют симптомы со стороны желудочно-кишечного тракта, у худощавых – респираторные проблемы [31]. Этот факт подтверждает и наше наблюдение. Больная была повышенного питания, и клиническая симптоматика отмечалась преимущественно со стороны пищеварительного тракта.
Точный диагноз ГМ базируется, главным образом, на данных рентгенологических методов исследования [4, 7-9]. В боковой проекции петля поперечной ободочной кишки располагается позади грудины и впереди печени, при этом отчетливо виден симптом «сдавления» или «перетяжки», свидетельствующий о наличии грыжевых ворот. При парастернальных грыжах, содержащих только сальник, в кардиодиафрагмальном углу обнаруживается округлое, гомогенное образование. Более информативна КТ [17, 25]. Однако и здесь при выявлении над диафрагмой массы с плотностью жира могут возникать трудности дифференциальной диагностики с липомой или липосаркомой [8, 17, 25, 27, 33]. Представленное наблюдение иллюстрирует трудности диагностики ГМ. Грыжа развивалась в течение 5-10 лет на фоне сопутствующих заболеваний: рецидивной вентральной грыжи и дефекта межпредсердной перегородки, симптомы которых маскировали клинические проявления диафрагмальной грыжи. Одышку при нагрузке, тяжесть и неясные боли за грудиной, диспепсические нарушения длительное время относили именно к проявлению сопутствующих заболеваний. Только в последние годы после рентгенографии органов грудной клетки было высказано предположение о наличии грыжи диафрагмы, а диагноз парастернальной грыжи установлен лишь при КТ.
Точная верификация диагноза важна для выбора оптимальной тактики лечения. Большинство хирургов едины во мнении, что грыжесечение необходимо проводить сразу после установления диагноза ГМ из-за реальной опасности ущемления органов брюшной полости или развития непроходимости [1, 2, 5, 7, 18, 22, 25, 35, 37]. Тем не менее в приведенном наблюдении, несмотря на выраженную симптоматику, больной было отказано в операции в двух центральных лечебных учреждениях из-за наличия у нее сопутствующего дефекта межпредсердной перегородки.
Крайне редки наблюдения сочетания ГМ с хирургическими заболеваниями сердца. Описаны единичные наблюдения ГМ, случайно выявленной во время кардиохирургических операций [21]. M. Huang и J. Young [19] провели протезирование аортального клапана, аортокоронарное шунтирование и пластику правосторонней ГМ у больной 76 лет. V. Saplacan и соавт. [29] сообщили об одномоментном грыжесечении и протезировании восходящей аорты у больного с синдромом Марфана. Мы нашли лишь одно сообщение о сочетании ГМ и дефекта межпредсердной перегородки у взрослого человека [10]. В нашем наблюдении необходимо было провести хирургическое лечение аневризмы межпредсердной перегородки в сочетании с множественными дефектами, большой левосторонней ГМ, рецидивной вентральной грыжей. Также необходимо было учитывать наличие аномального венозного дренажа из участка толстой кишки непосредственно в правое предсердие. Точная дооперационная диагностика позволила разработать оптимальный план оперативного вмешательства.
ГМ в большинстве наблюдений предпочтительно оперировать, используя трансабдоминальный доступ, менее травматичный, чем трансторакальный [1, 2, 5, 7, 18, 20, 37]. Объем вмешательства при ГМ стандартный. Содержимое грыжи выделяют и низводят в брюшную полость, мешок иссекают. При невозможности низведения сальника производят его резекцию. Дефект диафрагмы ликвидируют, подшивая ее край к грудной клетке или влагалищу прямой мышцы отдельными нерассасывающимися швами [5, 7, 23, 27]. При больших размерах грыжевых ворот ставят заплату из полипропиленовой сетки [12, 19, 21, 27]. Описаны варианты пластики через срединную стернотомию. Этот доступ выбирают при подозрении на опухоль переднего средостения или при сочетании ГМ с хирургическими заболеваниями сердца [10, 19, 21, 29]. У оперированной нами больной по данным КТ поперечная ободочная кишка плотно прилегала к грудине. Во избежание повреждения грыжевого содержимого, а также учитывая наличие рецидивной вентральной грыжи, первый этап операции провели, используя трансабдоминальный доступ с мобилизацией и низведением грыжевого содержимого в брюшную полость. Далее осуществили срединную стернотомию. Внутрисердечный этап операции протекал стандартно, хотя были определенные сложности при подключении аппарата искусственного кровообращения из-за наличия выраженного спаечного процесса в полости перикарда и аномального венозного сосуда, впадающего в правое предсердие. Несмотря на относительно большой дефект диафрагмы размером 10×5 см, нам удалось сшить края грыжевых ворот без существенного натяжения, тогда как повторная пластика брюшной стенки была выполнена с укреплением шва апоневроза сетчатым эндопротезом по типу on lay.
Таким образом, точная дооперационная диагностика всего комплекса анатомических нарушений позволила разработать и успешно провести одномоментное хирургическое вмешательство при редком сочетании диафрагмальной и вентральной грыж с хирургическими заболеваниями сердца.
Источник
Грыжа Морганьи
Пост опубликован: 13.12.2015
Между грудиной и реберными частями диафрагмы имеются участки большей или меньшей величины, лишенные мышечных волокон, где брюшина и плевра соприкасаются. В этих местах иногда образуются грыжи, называемые позадигрудинными (ретростернальными), парастернальными, субкостостернальными или грыжами через отверстие Морганьи или щель Ларрея. Они значительно чаще наблюдаются справа, чем слева, но могут быть и двусторонними, составляя около 3% всего числа диафрагмальных грыж.
Грыжи Морганьи рассматривают либо как врожденные, либо как развившиеся на почве врожденного предрасположения. Оба предположения нужно считать правильными. Иногда такие грыжи обнаруживают у маленьких детей, но гораздо чаще они образуются у людей в возрасте около 30 лет, особенно в случаях ожирения или похудания, в результате воздействия повышенного внутрибрюшного давления на ослабленный участок диафрагмы.
Симптомы грыжи Морганьи
Позадигрудинные грыжи всегда имеют грыжевой мешок. Обычным содержимым является сальник или участок толстой кишки, редко петля тонкой кишки или часть желудка. Такие грыжи могут длительней протекать бессимптомно; их обнаруживают случайно при рентгеноскопии. При большой величине грыжи могут возникнуть одышка, боль в груди, кашель или тошнота, рвота, запоры и, реже, явления частичной непроходимости кишечника.
При рентгенологическом исследовании устанавливается затенение почти правильной округлой формы, около 5—10 см в диаметре, что часто оценивается как опухоль либо эхинококк легкого, перикарда или печени, для постановки правильного диагноза имеет значение типичное расположение затенения, не имеющего четкого нижнего края, в диафрагмально- медиастинальном углу. Исследование в профильной проекции показывают, что образование расположено спереди, за грудиной. Находящийся в грыже Морганьи сальник дает гомогенную тень. Выхождение отрезка кишки может быть установлено при исследовании без применения контрастной взвеси, уточняется только при контрастировании.
Лечение грыжи Морганьи
Оперативное лечение таких грыж показано во всех случаях. Лапаротомия через прямую мышцу живота создает хороший доступ к грыжевым воротам. Вправление брюшных органов происходит большей частью легко. Для закрытия дефекта в диафрагме надсекают брюшину по краю грыжевых ворот. Мешок грыжи Морганьи может быть удален, если он легко низводится. Нет основания стремиться к этому во всех случаях. При небольшом дефекте края его сближают швами. При большом отверстии край дефекта диафрагмы подшивают к заднему листку прямой мышцы живота, к передней стенке грудной клетки. Для подкрепления линии швов может быть использована круглая связка печени.
Чресплевральный доступ при этом виде грыж не должен применяться. Он создает большие неудобства для хирурга, вынужденного иногда перейти к излишне травматичной торако-лапаротомии.
Источник статьи: https://surgeryzone.net/info/info-hirurgia/gryzha-morgani.html
Диафрагмальная грыжа
Диафрагмальная грыжа — это транспозиция брюшных органов в полость грудной клетки через отверстие в диафрагме. У некоторых пациентов протекает бессимптомно. Проявляется болью, урчанием в грудной клетке, диспепсией, дисфагией, при больших дефектах — нарушением сердечной деятельности и дыхания. Диагностируется с помощью рентгенографии грудной клетки, эзофагогастроскопии, внутрипищеводной pH-метрии. Для устранения диафрагмальных дефектов используют лапароскопическую фундопликацию, лапаротомную или торакотомную гастропексию, операции Ниссена, Белси, ушивание, пластику, аллопротезирование грыжевого отверстия.
МКБ-10
Общие сведения
Диафрагмальные грыжи были впервые описаны французским хирургом Амбруазом Паре в 1579 году, принадлежат к категории часто встречающихся болезней пищеварительного тракта, составляют до 2% всех видов грыжевых образований. Распространенность патологии возрастает от 10% в молодом возрасте до 50% у 50-60-летних пациентов. Заболевание диагностируют у 7-10% больных, предъявляющих жалобы на боли в груди и нарушения сердечной деятельности.
Врожденные грыжевые дефекты диафрагмы являются одной из распространенных причин мертворождения, выявляются у 1 из 2 000-4 000 живорожденных младенцев, часто сочетаются с другими пороками развития, составляют до 8% всех наследственных и дизэмбриогенетических аномалий.
Причины
Заболевание является полиэтиологическим. Во взрослом возрасте патология зачастую развивается при сочетании нескольких эндогенных или экзогенных провоцирующих факторов, врожденное грыжевое выпячивание формируется в результате генетических мутаций. Специалисты в сфере хирургии и гастроэнтерологии называют следующие группы причин и предпосылок возникновения грыж диафрагмы:
- Аномалии диафрагмальных мышц и пищевода. Недоразвитие отдельных участков и аплазия части диафрагмы может иметь как наследственное, так и дизэмбриогенетическое происхождение. Семейные формы пороков развития, в том числе укорочение пищевода, вероятнее всего наследуются по мультифакторному или аутосомно-рецессивному типу. Грыжи диафрагмальной локализации в сочетании с гипоплазией пальцев, расщеплением неба и верхней губы выявляются у пациентов с синдромом Фринса. Возможной причиной дефекта является воздействие вирусных и токсических мутагенов на 8 неделе гестации.
- Дисплазия соединительной ткани. Наследуемое нарушение синтеза и пространственной организации коллагена, эластина, белково-углеводных комплексов проявляется снижением прочности и повышением эластичности соединительнотканных волокон. При повышении нагрузок на диафрагмальные участки с ослабленными волоконными структурами возможно их растяжение, формирование дефектов. Подтверждением диспластического происхождения части грыж диафрагмы считается сочетание патологии с варикозной болезнью, геморроем, миопией, сколиозом, другими врожденными коллагенопатиями.
- Травматические повреждения диафрагмы. Нарушение целостности диафрагмальных волокон наблюдается при резких ударах в область ребер и живота со значительным смещением пищевода, верхней части желудка, проникающих колотых, режущих, огнестрельных ранах грудной и брюшной полости. У части пациентов грыжа развивается после выполнения операций на диафрагме — чресплевральной, сагиттальной, срединной чрезбрюшинной диафрагмотомии, проводимой для ревизии органов верхнего этажа брюшной полости, при раке желудка, пищевода, резекции печени, дренировании заднего средостения и др.
- Повышение давления в брюшной полости. Играет ключевую роль при наследственной дисплазии соединительной ткани. Вероятность образования грыжи возрастает при тяжелых физических нагрузках, запорах, ожирении, крупных неоплазиях брюшных органов, асцита. Наличие диафрагмальных грыжевых образований подтверждается почти у половины пациентов, страдающих рецидивирующей бронхолегочной патологией с сухим надсадным кашлем (хроническим бронхитом, бронхиальной астмой). В группу риска входят женщины, выносившие многоплодную беременность или родившие нескольких детей.
- Хронические заболевания ЖКТ. Язва желудка, двенадцатиперстной кишки, хронический холецистит, панкреатит могут осложняться гипермоторной дискинезией. В результате продольных сокращений мускулатуры пищевода происходит вертикальная тракция органов ЖКТ, увеличивается нагрузка на фасциальные связки, диафрагмальные сухожилия, растягивается пищеводное отверстие диафрагмы. Аналогичная ситуация возникает при хронических эзофагитах со стойким воспалительным спазмом мышечных волокон или рубцовом укорочении органа после химических, термических, лучевых ожогов.
По мнению ряда авторов, образованию грыж способствует возрастное снижение тонуса диафрагмальных мускульных волокон, мышечная дистрофия после осложненных родов, тяжелых интоксикаций, сепсиса, других неотложных состояний. При нарушениях иннервации происходит локальная релаксация мышцы с образованием так называемых диафрагмальных невропатических грыж.
Патогенез
В основе механизма диафрагмального грыжеобразования лежит расширение естественных отверстий, наличие или возникновение патологических дефектов в диафрагме с перемещением через них в торакальную полость пищеварительных органов. Из трех анатомических отверстий в формировании грыжевых выпячиваний участвует только пищеводное, через которое внутрь грудной полости втягивается гастроэзофагеальный переход с кардиальной частью желудка (скользящая диафрагмальная грыжа) либо желудочное дно, тело, реже — другие отделы органа, петли тонкого кишечника (параэзофагеальная грыжа).
При аплазии мышечных волокон, врожденном расщеплении соединительной ткани в так называемых слабых зонах (люмбокостальная грыжа Бохдалека, ретрокостостернальная грыжа Ларрея-Морганьи, ретростернальные грыжи) дефект диафрагмы существует изначально. Травматические воздействия, высокое абдоминальное давление, локальное мускульное расслабление провоцируют образование патологических диафрагмальных отверстий.
Нетравматические приобретенные грыжевые выпячивания чаще возникают при врожденных коллагенопатиях, способствующих растяжению сухожильных волокон и фасциальных связок. Смещение брюшных органов, их сдавление краями диафрагмальных отверстий, компрессия легких и сердца приводят к формированию характерной клинической картины заболевания.
Классификация
Систематизация форм диафрагмальных грыж учитывает время их возникновения, структуру грыжевого выпячивания, этиологию, локализацию. Такой подход обоснован различием клинической симптоматики, прогноза, врачебной тактики при разных видах заболевания. С учетом основных критериев классификации гастроэнтерологи и общие хирурги различают следующие варианты патологии:
- По времени возникновения: врожденные и приобретенные грыжи. Наследственные и дизонтогенетические грыжевые образования встречаются реже, однако отличаются более тяжелой клиникой и серьезным прогнозом. Грыжи, сформировавшиеся постнатально, зачастую протекают с менее выраженными клиническими симптомами или латентно.
- По структуре грыжевого выпячивания: истинные и ложные грыжи. У истинных грыж есть грыжевой мешок, образованный пристеночными брюшиной и плеврой. У ложных грыжевой мешок отсутствует, а смещенные брюшные органы свободно двигаются внутри грудной клетки. Прогностически более благоприятными считаются истинные грыжевые образования.
- По происхождению и локализации: травматические и нетравматические грыжи. Нетравматические выпячивания бывают ложными врожденными, истинными слабых зон, истинными атипичной локализации, скользящими и параэзофагеальными пищеводного отверстия диафрагмы. В 90% случаев патология представлена грыжами в области отверстия пищевода.
Симптомы диафрагмальных грыж
Клинические проявления заболевания связаны с нарушением работы ЖКТ, дыхательной и сердечно-сосудистой систем. Возможные диспепсические расстройства при грыже представлены отрыжкой воздухом или кислым, постоянной изжогой, которая может усиливаться после еды или при наклонах туловища, метеоризмом, рвотой, не приносящей облегчения.
Характерный симптом — «бульканье» или урчание в груди. Вследствие раздражения диафрагмальных нервов пациентов беспокоят интенсивные загрудинные боли, иррадиирующие в плечо. Также наблюдается тахикардия после приема пищи, одышка, трудности при проглатывании жидкой пищи, ощущение «комка». При небольшом размере грыжи симптоматика болезни может отсутствовать или быть очень скудной.
Для врожденной патологии характерно развитие клинической картины уже в период новорожденности. Клиника зависит от размеров дефекта диафрагмальных тканей. При тяжелом течении симптоматика возникает в первые часы после родов и включает такие проявления, как цианоз кожных покровов, асимметрия грудной клетки, срыгивания, отказ от кормления, дефицит массы тела, нарушения сна, постоянный плач.
У части младенцев из-за смещения брюшных органов формируется ладьевидный живот. При небольших грыжевых отверстиях симптомы грыжи развиваются позже, иногда в позднем детстве после перенесенного инфекционного энтерита, напоминают клинику заболевания у взрослых.
Осложнения
Вследствие расширения пищеводных вен могут возникать острые кровотечения, проявляющиеся кровавой рвотой или меленой. У 50% больных из-за постоянного попадания агрессивного содержимого желудка на слизистую нижней трети пищевода диафрагмальная грыжа эзофагеального отверстия осложняется рефлюкс-эзофагитом (ГЭРБ). Длительное течение ГЭРБ сопровождается метаплазией эпителия с последующей возможной малигнизацией клеток.
Сдавление грыжевого мешка в диафрагмальном отверстии провоцирует ущемление грыжи, при котором наблюдаются процессы ишемии и некроза тканей смещенных органов, возрастает риск вовлечения в деструктивно-воспалительный процесс брюшины с развитием перитонита. В редких случаях грыжа осложняется аспирационной пневмонией. При длительном сдавлении легких, сердца нарастает дыхательная и сердечная недостаточность.
Диагностика
Постановка диагноза диафрагмальной грыжи зачастую затруднена, что обусловлено многообразием и неспецифичностью клинических проявлений, которые могут наблюдаться при других патологических состояниях. Диагностический поиск направлен на подтверждение наличия выпячивания, оценку содержимого грыжевого образования. План обследования пациента включает такие методы, как:
- Рентгенография грудной клетки. Проведение рентгенологического исследования ОГК с контрастным веществом в положении больного по Тренделенбургу считается «золотым стандартом» для диагностики грыжи. Рентгенограмма позволяет оценить локализацию и размеры диафрагмального дефекта, визуализировать интраторакальное проникновение органа или его части.
- Эзофагогастроскопия. Гастроскопия обеспечивает осмотр слизистой оболочки верхних отделов пищеварительного тракта, оценку степени ее повреждения. О наличии грыжи косвенно свидетельствует укорочение расстояния до нижнего пищеводного сфинктера, неполное смыкание кардии желудка, сглаженность складок слизистой клапана Губарева.
- Определение кислотности. Внутрипищеводная рН-метрия помогает верифицировать диагноз рефлюкс-эзофагита, который является самым распространенным осложнением грыжи диафрагмы. Дополнительно проводится кислотно-перфузионный тест Бернштейна с введением в пищевод слабого раствора соляной кислоты, что вызывает усиление симптомов у больных с ГЭРБ.
Лабораторные исследования при грыже диафрагмы недостаточно информативны, поскольку отклонения показателей от нормы обусловлены присоединившимися осложнениями. Для комплексной оценки состояния пищеварительной системы рекомендованы УЗИ, КТ, МСКТ брюшной полости. С целью исключения сердечной патологии выполняется ЭКГ с велоэргометрической пробой, эхокардиография.
Грыжи диафрагмы необходимо дифференцировать с язвой желудка, пилоростенозом, кишечной непроходимостью, рубцовыми эзофагеальными стриктурами, злокачественными новообразованиями пищевода, кардии, ишемической болезнью сердца, абсцессами и кистами легких, экссудативным плевритом, легочной формой туберкулеза, опухолями средостения, повреждениями диафрагмального нерва.
Лечение диафрагмальных грыж
Радикальным методом, позволяющим излечить заболевание, является герниопластика. От операции можно воздержаться при выявлении бессимптомной скользящей грыжи эзофагеального отверстия диафрагмы, обеспечив пациенту диспансерное наблюдение. В остальных случаях смещенные органы в ходе хирургического вмешательства низводятся в брюшную полость, после чего устраняется диафрагмальный дефект при ложных грыжевых образованиях или выполняется пластика при истинных. Новорожденным с выраженной компрессией органов грудной полости операция осуществляется в экстренном порядке. У взрослых герниопластику обычно проводят планово.
При длительно существующих грыжах, осложненных хроническими заболеваниями органов ЖКТ, рекомендовано комбинированное лечение с коррекцией диеты, назначением противоязвенной, противовоспалительной, заместительной энзимной, антибактериальной, прокинетической, спазмолитической, другой этиопатогенетической и симптоматической медикаментозной терапии. Рекомендованными видами вмешательств являются:
- Эндоскопические методики. Лапароскопическая фундопликация применим при грыжевом выпячивании через эзофагеальное отверстие диафрагмы. Формирование околопищеводной муфты из дна желудка с фиксацией к диафрагме и сужением диафрагмального отверстия позволяет устранить грыжевой дефект и восстановить запирательную функцию кардиального сфинктера. Преимуществами лапароскопического вмешательства являются низкая травматичность, сокращение длительности операции, более быстрое послеоперационное восстановление пациента.
- Лапаротомная и торакотомная герниопластика. При параэзофагеальных и скользящих грыжах выполняют гастрокардиопексию, операцию Белси, фундопликацию по Ниссену, Тупе. У остальных пациентов при небольших диафрагмальных отверстиях целостность ткани восстанавливают методом создания дупликатуры. Для устранения больших дефектов проводят аллопластику с установкой нейлонового, тефлонового, капронового протеза. Грыжесечение ущемленной грыжи предполагает ревизию содержимого грыжевого мешка с резекцией нежизнеспособных тканей.
Прогноз и профилактика
При ранней диагностике и адекватной терапии выздоровление наступает у большинства больных. Прогноз относительно благоприятный. В дальнейшем повышается риск развития рецидивов грыжи, особенно после оперативного вмешательства по укрепле