Аллопластический материал при лечении грыжи

- Авторы
- Резюме
- Файлы
- Ключевые слова
Васильев М.Н., Ванюшин П.Н., Григорьев К.Ю., Морозов В.С.
Предложен способ комбинированной аллогерниопластики послеоперационных срединных вентральных грыж. Предусмотренное этим способом расположение эксплантата внутри дупликатуры, образованной листками и лоскутами влагалищ прямых мышц живота, позволяет исключить вероятность развития осложнений, характерных для подкожного и предбрюшинного расположения эксплантата. С использованием предлагаемого способа оперировано 7 пациентов, получены удовлетворительные результаты, рецидивов не отмечено.
послеоперационная грыжа
аллопластика
Введение
Лечение послеоперационных вентральных грыж остается актуальной задачей абдоминальной хирургии. Это заболевание возникает у 2‒20 % больных, перенесших лапаротомию, и по частоте занимает второе место после паховых грыж [2]. В современной герниологии чаще используют синтетические материалы [4].
Частота раневых осложнений после пластики передней брюшной стенки по поводу послеоперационной вентральной грыжи варьирует от 20,9 до 67 % [4]. Существует мнение, что применение сетчатых протезов увеличивает частоту раневых осложнений.
В настоящее время при пластике грыж эндопротез используют в одном из нескольких вариантов расположения по отношению к мышечно-апоневротическому слою передней брюшной стенки on lay или sub lay.
Основным недостатком пластики сетчатым протезом является развитие послеоперационных осложнений: нагноение, серома, гематома, отторжение протеза, формирование кишечных спаек и свищей [3‒5].
Эти обстоятельства побудили нас искать способ, позволяющий улучшить результаты лечения послеоперационных вентральных грыж, снизив количество послеоперационных осложнений.
Цель исследования
Оценить результаты применения разработанного способа пластики передней брюшной стенки у больных с послеоперационными срединными вентральными грыжами.
Материал и метод исследования
В исследование были включены 50 больных, оперированных в плановом порядке в хирургическом отделении ГУЗ УОКБ за период с 2007 по 2010 гг. Все пациенты были женского пола, у всех грыжи сформировались после верхнесрединной лапаротомии. В основную группу вошли 7 пациентов, оперированных по разработанной нами методике (заявка на изобретение № 2010112912). В контрольную группу включили 43 пациента, оперированных по методике on lay. Обе группы были сопоставимы по возрасту (средний возраст в основной группе – 56,57 лет, средний возраст в контрольной группе – 57,65 лет), размерам грыжевого дефекта (по классификации J.Chevrel-A.Rath, в основной группе W1 – 2 больных (28,8 %), W2 – 5 больных (71,2 %); в контрольной группе W1 – 13 больных (30,2 %), W2 – 30 больных (69,8 %)). В основной группе различная сопутствующая патология встречалась у 4 пациентов (57,14 %), в контрольной группе – у 27 (62, 8 %).
Разработанный нами метод осуществляется следующий образом. Двумя окаймляющими разрезами в проекции грыжи рассекают кожу с подкожной клетчаткой (рис. 1, 2), выделяют грыжевой мешок до грыжевых ворот. Грыжевой мешок вскрывают и выполняют внутрибрюшной этап операции (рассечение спаек, ликвидация непроходимости, симультанные операции на внутренних органах). Потом производят сшивание без натяжения между собой брюшины и рассеченных оболочек грыжевого мешка, в зависимости от размеров, «край в край» или с формированием дупликатуры.
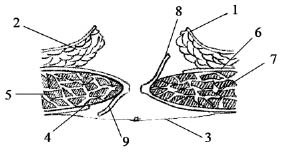
Рис. 1. 1 – кожа; 2 – подкожная клетчатка;
3 – лоскут переднего листка влагалища левой прямой мышцы живота; 4 – передний листок влагалища
левой прямой мышцы живота; 5 – левая прямая
мышца живота; 6 – ушитые листки брюшины;
7 – лоскут заднего листка влагалища правой прямой мышцы живота; 8 – задний листок влагалища
правой прямой мышцы живота;
9 – правая прямая мышца живота
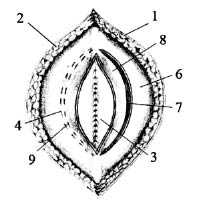
Рис. 2. 1 – кожа; 2 – подкожная клетчатка; 3 – лоскут переднего листка
влагалища левой прямой мышцы
живота; 4 – передний листок
влагалища левой прямой мышцы
живота; 6 – ушитые листки брюшины; 7 – лоскут заднего листка влагалища правой прямой мышцы живота;
8 – задний листок влагалища правой прямой мышцы живота;
9 – правая прямая мышца живота
Необходимый участок заднего листка влагалища правой прямой мышцы живота освобождают на всю длину грыжевого дефекта, отслаивая подлежащую брюшину. Необходимый участок переднего листка влагалища левой прямой мышцы живота освобождают от подкожной клетчатки на всю длину грыжевого дефекта.
Таким образом, изолировав брюшную полость и освободив необходимые участки листков влагалищ прямых мышц живота, переходят непосредственно к пластике.
Сначала, отступив на 1-1,5 см от края грыжевых ворот, выполняют полуовальный разрез переднего листка влагалища левой прямой мышцы живота на всю длину грыжевого дефекта, затем такого же размера полуовальный разрез заднего листка влагалища правой прямой мышцы живота (рис. 1, 2). Расправляют лоскут переднего листка влагалища левой прямой мышцы живота и лоскут заднего листка влагалища правой прямой мышцы живота.
Затем расправленный лоскут переднего листка влагалища левой прямой мышцы живота сшивают с задним листком влагалища правой прямой мышцы живота.
После этого выкраивают сетчатый эксплантат в виде буквы Н. Размеры сетчатого эксплантата по ширине превышают на 1-2 см края швов лоскутов влагалищ прямых мышц живота, а по длине – на 1,5-2 см больше грыжевого дефекта. Формируют ложе для расположения сетчатого эксплантата, образованное расправленным лоскутом переднего листка влагалища левой прямой мышцы живота и задним листком влагалища правой прямой мышцы живота путем частичного отслаивания правой и левой прямых мышц живота. Сетчатый эксплантат укладывают под правую и левую прямые мышцы живота на сформированное ложе, верхние и нижние концы сетчатого эксплантата располагают за края ушитого дефекта в соответствующих влагалищах прямых мышц живота и без натяжения подшивают его по периметру и по центру к сформированному ложу с помощью синтетических нитей редкими узловыми швами. Затем поверх сетчатого эксплантата правой и левой прямых мышц живота ушивают расправленный лоскут заднего листка влагалища правой прямой мышцы живота с передним листком влагалища левой прямой мышцы живота (рис. 3, 4). Таким образом, формируют дупликатуру, образованную листками и лоскутами влагалищ прямых мышц живота. Операцию завершают установкой дренажей внутри дупликатуры для последующей вакуумной аспирации. Кожную рану зашивают.
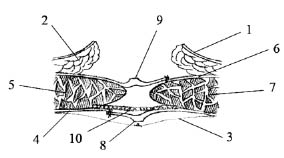
Рис. 3. 1 – кожа; 2 – подкожная клетчатка;
3 – лоскут переднего листка влагалища левой прямой мышцы живота; 4 – передний листок влагалища левой прямой мышцы живота; 5 – левая прямая мышца
живота; 6 – ушитые листки брюшины; 7 – лоскут
заднего листка влагалища правой прямой мышцы
живота; 8 – задний листок влагалища правой прямой мышцы живота; 9 – правая прямая мышца живота;
10 – имплантат (эндопротез)
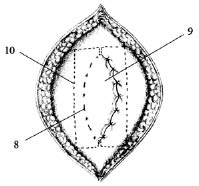
Рис. 4. 8 – задний листок влагалища правой прямой мышцы живота;
9 – правая прямая мышца живота;
10 – имплантат (эндопротез)
В качестве сетчатого эксплантата в обеих группах использовались полипропиленовая сетка и шовный материал пролен.
Все пациенты проходили тщательное догоспитальное обследование и осмотр смежных специалистов. Проводилась предоперационная подготовка с учетом сопутствующей патологии. Всем больным проводилась неспецифическая профилактика тромбоэмболических осложнений: эластическая компрессия нижних конечностей, ранняя активизация больных. При наличии факторов риска производилось введение низкомолекулярного гепарина: начиная с первых 12 часов после операции и в течение 5-7 дней послеоперационного периода. Для профилактики послеоперационных раневых осложнений за 30 минут до операции или интраоперационно вводились антибиотики цефалоспоринового ряда. Во всех случаях выполнялось дренирование раны в течение 2-5 дней. В послеоперационном периоде выполнялся ультразвуковой контроль течения раневого процесса на 3, 10 сутки.
Результаты исследования и их обсуждение
Среднее количество койко-дней в основной группе было 12,3, в контрольной группе – 16,26. В основной группе раневых послеоперационных осложнений не наблюдалось. В контрольной группе осложнения отмечены у 7 – (16,28 %) пациентов. У 2 – (4,66 %) – длительная серозная экссудация из раны, у 1 – (2,33 %) некроз краев раны, у 1 – (2,33 %) инфильтрат. Гематома наблюдалась у 3 – (6,96 %) пациентов контрольной группы, из которых в одном случае гематома была инфицированная. При анализе причин инфицирования было выяснено, что присутствовала инфекция в зоне оперативного вмешательства (гнойные гранулемы). В послеоперационном периоде в контрольной группе умерла 1 (2,33 %) больная от острого нарушения мозгового кровообращения. Летальных случаев в основной группе не было. Рецидивов грыж в обеих группах не отмечено (сроки наблюдения основной группы
9 месяцев, контрольной группы до 3 лет).
Выводы
Использование предложенного способа позволяет выполнить пластику дефектов стенки живота без значительного уменьшения объема брюшной полости, уменьшить число послеоперационных раневых осложнений и летальных исходов.
Список литературы
- Войленко В.Н., Меделян А.И., Омельченко В.М. Атлас операций на брюшной стенке и органах брюшной полости – М.: Медицина, 1965. – 608 с.
- Деметриашвили З.М., Магалашвили Р.Д., Лобжанидзе Г.В. Лечение послеоперационных вентральных грыж// Хирургия. – 2008. – №11. – С. 44-46.
- Загиров У.З., Салихов М.А., Исаев У.М. Анатомо-функциональное обоснование нового способа комбинированной пластики срединных вентральных грыж // Хирургия. – 2008. – №7. – С. 41-42.
- Мирзабекян Ю.Р., Добровольский С.Р. Прогноз и профилактика раневых осложнений после пластики передней брюшной стенки по поводу послеоперационной вентральной грыжи // Хирургия. – 2008. – №1. – С. 66-71.
- Нелюбин П.С., Галота Е.А., Тимошин А.Д. Хирургическое лечение больных с послеоперационными и рецидивными вентральными грыжами // Хирургия. – 2007. – №7. – С. 69-74.
- Тоскин К.Д., Жебровский В.В. Грыжи живота. – М.: Медицина, 1983. – 240 с.
Библиографическая ссылка
Васильев М.Н., Ванюшин П.Н., Григорьев К.Ю., Морозов В.С. СПОСОБ АЛЛОПЛАСТИКИ ПОСЛЕОПЕРАЦИОННЫХ ВЕНТРАЛЬНЫХ ГРЫЖ // Фундаментальные исследования. – 2010. – № 11. – С. 33-36;
URL: https://fundamental-research.ru/ru/article/view?id=14012 (дата обращения: 20.08.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Грыжа – это патологическое выпячивание органа либо его части под кожу, во внутренние полости, межмышечные пространства через естественные (щели в белой линии живота, пупочное кольцо) или приобретённые отверстия в тех или иных анатомических образованиях (так называемые «слабые места»). Элементами наружной грыжи живота являются грыжевые ворота, грыжевой мешок и грыжевое содержимое.
Грыжевые ворота ограничивают собой грыжевой дефект и могут иметь размер от нескольких сантиметров в диаметре (в основном при грыжах белой линии живота и пупочных) до двадцати-тридцати сантиметров и даже более, что чаще всего встречается при послеоперационных грыжах и диастазе (расхождении) прямых мышц живота.
В основном в грыжевой мешок выходят подвижные органы брюшной полости, а именно: петли тонкой кишки (чаще всего), сальник (несколько реже), слепая кишка, аппендикс, поперечно-ободочная и сигмовидная кишка, меккелев дивертикул и т.д.
Особенностью внутренних грыж живота (лат. hernia abdominalis interna) является то, что в число их элементов не входит грыжевой мешок, он здесь попросту отсутствует. Выпячиваться через грыжевые ворота в подобных ситуациях могут быть не только вышеперечисленные органы, но также желудок, селезёнка, печень и почки.
Особенности оперативного лечения пупочных грыж
На сегодняшний день вылечить пупочную грыжу у взрослых пациентов можно лишь посредством хирургического вмешательства. Если нет ущемления образования, и оно свободно вправляется, можно ограничиться ушиванием пупочного кольца. При сильном расширении для закрытия используют пластику.
При развитом некротическом процессе, а именно, при омертвении тканей органа, замкнутого в грыжевом мешке, требуется больший объем оперативного вмешательства. В этом случае врач удаляет измененные участки.
Существует множество способов герниопластики: Сапежко, Мейо, Лекстеру и т. д. Различия, в основном, заключается в способе доступа, остальные этапы практически идентичные
Современные технологии лечения грыж живота
На современном этапе в герниологии для пластики дефектов брюшной стенки в подавляющем большинстве случаев применяются искусственные материалы.
Эндопротезы представляют собой мелкоячеистые сетчатые пластини. Крепятся они по типу заплаты специальными нитями, скобами или «липучками» в области грыжевых ворот. При этом дефект покрывается с избытком, вследствие чего предупреждается натяжение и повреждение окружающих тканей. Достаточно три-четыре недели после операции, чтобы сетчатый имплантат пророс соединительной тканью и стал надежной защитой для профилактики развития рецедива заболевания. Вариантов данной операции несколько. Это и способ Лихтенштейна (Lichtenstein), и Шоудайса (Shouldice), и лапароскопический подход – каждый из них имеет свои показания.
Суть метода заключается в выкраивании из специального материала индивидуального по своим размерам и форме лоскута, который затем надёжно фиксируется в виде заплаты к тканям брюшной стенки либо нерассасывающимися монофиламентными, проленовыми нитями достаточной толщины, либо танталовыми скрепками, накладывающимися специальным степлером. Помимо этого сейчас выпускаются сетки, изначально снабжённые особыми липучками для крепления – их не пришивают, а просто прижимают к окружающим тканям.
В работе используются ультрасовременные аллопластические материалы. Они позволяют значительно снизить риск повторного возникновения грыжи, он равен всего лишь 1%. Пластичный сетчатый имплантат берет на себя всю нагрузку. При этом ткани при его установке не стягиваются, благодаря чему уменьшается выраженность болевого синдрома. Ненатяжная герниопластика сводит к минимуму вероятность возникновения осложнений после операции и сокращает продолжительность реабилитации пациентов.
Также возможно проведение герниопластики местными тканями. Этот способ применяется только у молодых пациентов с неосложненными грыжами небольших размеров.
Лечение паховой грыжи
Развитие паховой грыжи может повлечь за собой опасные для жизни осложнения. Поэтому ее лечение не обходится без хирургического вмешательства. При этом совсем не важно, каков тип выпячивания и какого размера образование.
Существует два основных способа удаления паховой грыжи:
Открытый способ удаления грыжи
Открытый – это удаление грыжи проводится через наружный разрез брюшной стенки непосредственно в месте грыжевого выпячивания. Ранее такая операция называлась грыжесечением, что не совсем правильно – ведь грыжа не иссекается. Она вправляется на свое место. А основная цель операции – ушивание грыжевых ворот и укрепление (пластика) слабых мест. Поэтому сейчас все чаще применяется термин «герниопластика».
Лапароскопическая герниопластика
Лапароскопический – грыжа удаляется «изнутри», посредством лапароскопа, введенного через небольшие проколы в брюшную полость. Лапароскопические вмешательства производятся не через разрез, а через проколы брюшной стенки.
В современной медицине используют два варианта герниопластики: натяжную и ненатяжную. Первый предполагает закрытие дефекта брюшной стенки с помощью стягивания собственных тканей и сшивания их между собой. Второй подразумевает установку синтетического эндопротеза.
Имплантат изготавливается из высокотехнологичных полимерных материалов. Он обеспечивает сохранение естественных пропорций в паховом канале, исключает натяжение тканей и способствует уменьшению болевого синдрома. Восстановление пациентов при ненатяжной герниопластике происходит намного быстрее. К тому же имплантацию синтетического эндопротеза можно осуществлять и лапароскопическим способом.
Источник
Аллопластические способы операции при паховых грыжах. Эти способы применяют при сложных паховых грыжах. В настоящее время клиническую апробацию прошло огромное количество пластических материалов, но лишь немногие из них могут быть рекомендованы для широкого применения на практике. При лечении паховых грыж хорошие клинические результаты удается достигнуть с помощью аутотрансплантатов кожи [Янов В. Н., 1970; Кисель А. Г., 1974], аллотрансплантатов твердой мозговой оболочки [Зяблов В. И. и др., 1975; Шорлуян П. М., Химичев В. Г., 1978; Тоскин К. Д., Жебровский В. В., 1980] и ксенотрансплантатов брюшины [Шустеров А. И., 1967]. Из синтетических материалов хорошо зарекомендовал себя лавсан, фторлон и капрон [Туровец И. Г., 1974; Даурова Т. Т. и др., 1975; Жигалкина И. Я., 1977], а за рубежом— марлекс и полихлорвинил [Bronstein В., 1970; Baumber С, 1971]. Статистические данные, приведенные в табл. 7, касающиеся применения перечисленных пластических материалов исключительно при сложных формах паховых грыж, свидетельствуют о резком снижении количества рецидивов.
Аутодермальные трансплантаты готовят во время операции. Эллипсоидным разрезом в подвздошно-паховой области (на месте операции) иссекают лоскут кожи с подкожной клетчаткой размером 2×7 см, который однократно обрабатывают горячим (90°С) изотоническим раствором хлорида натрия. После такой термической обработки эпидермальный слой кожи легко снимают с помощью скальпеля. Подкожную жировую клетчатку иссекают с помощью изогнутых ножниц. Лоскут перфорируют скальпелем в шахматном порядке. Приготовленный таким образом трансплантат опускают в раствор пенициллина (1 000 000 ЕД пенициллина на 100 мл изотонического раствора хлорида натрия), где сохраняют его до начала аутодермопластики. Этот метод приготовления аутоде-рмальных трансплантатов разработан В. Н. Яновым (1970).
Аллотрансплантаты твердой мозговой оболочки заготавливают от трупов людей в возрасте от 18 до 59 лет, умерших скоропостижно. Забор материала производят в нестерильных условиях через 2—8 ч после смерти донора в соответствии с инструкцией Министерства здравоохранения СССР от 2.1.62 г. Согласно этой инструкции, взятие биологической ткани от трупа для целей пластики возможно у лиц мужского и женского пола, погибших в результате травм, инфаркта миокарда, атеросклероза, гипертонической болезни, электротравмы, отравления этиловым спиртом, самоповешения, высоких вывихов и переломов шейного отдела позвоночника. К противопоказаниям отнесены все случаи новообразований, туберкулез и другие инфекционные, а также септические заболевания. Заключение о пригодности трансплантатов к клиническому применению дают после получения результатов патологоанатомического исследования, данных о количестве билирубина, результатов реакции Вассермана и определения групповой принадлежности крови донора.
Для стерилизации трансплантатов могут быть применены: β-пропилактон, окись этилена, слабые (0,25, 0,5, 0,75, 1, 2%) растворы формалина. Бактерицидное действие Р-пропилактона и окиси этилена обеспечивает стерильность трансплантатов при 1—3-часовой экспозиции. Длительность стерилизации в слабых растворах формалина находится в прямой зависимости от его концентрации. Если трансплантаты, находящиеся в 1,2% растворах формалина,становятся стерильными в течение 6—8 ч, то при концентрации 0,25, 0,5, 0,75% необходимо проводить стерилизацию в течение 3—5 сут. Консервация твердой мозговой оболочки может быть различной, что зависит от технической оснащенности операционного блока. Одинаково хорошие результаты можно получить при консервации методом лиофилизации, замораживания в жидких и газообразных средах [Савельев В. И., 1978]. Мы широко применяли очень простой способ консервации трансплантатов в холодоустойчивой жидкости 31Е. Ее состав: цитрат натрия — 1 г, глюкоза — 3 г, бромид натрия — 0,2 г, спирт 95% — 10 мл, глицерин — 15 мл, дистиллированная вода — 90 мл. В этом консерванте пластический материал можно хранить в течение 6 мес. Перед употреблением трансплантат переносят в стерильный изотонический раствор хлорида натрия, где его содержат в течение 2—3 ч.
Ксеногенные трансплантаты брюшины заготавливают на мясокомбинате от только что забитых животных (быки, коровы). Листы париетальной брюшины тщательно очищают от жира, промывают в проточной воде с мылом и помещают в стерильные стеклянные банки с 2% водным раствором хлорамина. Через 2 сут брюшину вновь промывают и опять помещают в 2% раствор хлорамина, который сменяют ежедневно в течение. 12 сут. После этого пластическая ткань становится стерильной и годной к употреблению [Шустеров А. И., 1967]. Консервированную ксеногенную брюшину хранят в банках в 2% растворе хлорамина при температуре + 4—5°С. Срок хранения — 8—10 мес.
Рекомендуемая для пластики пахового канала синтетическая ткань (лавсан) должна соответствовать следующим характеристикам [Даурова Т. Т., 1974]: лавсановая трикотажная безузелковая сетка — нить № 200, размер ячеек — 1,5—2,0 мм, толщина перегородки — 0,1—0,15 мм, разрывная прочность по длине — 9—11 кг, по ширине — 20—25 кг.
Таблица 7. Частота рецидивов при аллопластических методах оперирования сложных форм паховых грыж

Раскрой синтетической ткани следует вести по одному ряду ячеек, расположенных взаимноперпендикулярно в горизонтальном и вертикальном направлениях. Перед стерилизацией протезную ткань необходимо выстирать в одном из синтетических моющих средств и тщательно, многократно прополоскать в проточной воде. Стерилизацию проводят двухкамерным кипячением в дистиллированной воде в течение 20 мин или автоклавирова-нием при 1,2—1,5 атм в течение 20 мин. Стерильность ткани должна быть подтверждена бактериологическими исследованиями. Стерильную сетку можно хранить в этиловом спирте (96%) в темной герметически закрытой стеклянной посуде при комнатной температуре.
Существуют два основных варианта применения пластического материала: укрепление трансплантатом передней и задней стенки пахового канала. При первом варианте пластики не исключается применение общепринятых способов Жирара, Спасокукоцкого и Кимбаровского, а лишь создаются дополнительные условия для их успешного выполнения. Примером таких операций могут служить способы Петровского — Бабичева — Николаева (рис. 25) и Костина (рис. 26). Методика имплантации по отношению к подкожной жировой клетчатке, апоневрозу или мышцам принципиального значения не имеет. Важен сам факт — укрепление только передней стенки пахового канала, что применительно к сложным паховым грыжам недостаточно.

Рис. 25. Способ Петровского — Бабичева — Николаева. Трансплантат пришивается внутри пахового канала снизу к паховой связке, сверху — к внутренней стороне верхнего лоскута апоневроза наружной косой МЫШЦЫ.

Рис. 26. Способ Костина. Трансплантат подшит к верхнему лоскуту апоневроза наружной косой мышцы и вместе с ним — к пупартовой связке.
Второй вариант пластики — укрепление задней стенки пахового канала. Метод детально разработали И. Г. Туровец (1965), Н. В. Воскресенский и С. Л. Горелик (1969), А. Г. Кисель (1974). После удаления грыжевого мешка осуществляют реконструкцию задней стенки пахового канала и формирование глубокого пахового кольца. Излишки поперечной фасции экономно иссекают и края ее тщательно ушивают узловыми швами. В латеральном отделе формируют глубокое кольцо пахового канала. Если поперечная фасция полностью разрушена, что обычно наблюдается при многократно рецидивирующих грыжах, следует максимально использовать рубцовые ткани. Более надежно и анатомично располагать трансплантат под мышцами, подшивая его в виде заплаты, замещающей прилежащий отдел поперечной фасции. Размер трансплантата обычно 6×8 см. Снизу трансплантат подшивают к паховой связке, сверху — к внутренней косой и поперечной мышцам, позади них (рис. 27). Швы проводят через мышцы и завязывают над ними. Затем на трансплантат укладывают семенной канатик и над ним создают дубликатуру апоневроза наружной косой мышцы живота. Преимущество этого метода в том, что внутреннюю косую и поперечную мышцы не используют для пластики задней стенки канала, что позволяет максимально сохранить их функцию и предупредить дальнейшее разрушение. Однако чаще трансплантат располагают поверх мышц (рис.28), фиксируя его швами сверху к передней стенке влагалища прямой мышцы живота, снизу — к паховой связке, внутренний край — к пупартовой связке и лонному бугорку, а латеральный — к передней поверхности внутренней косой мышцы.

Рис. 27. Укрепление трансплантатом задней стенки пахового канала по Воскресенскому — Горелику.

Рис 28. Укрепление трансплантатом задней стенки пахового канала по Киселю.
Важной технической деталью является тщательное расправление трансплантата. Необходимо добиваться его равномерного прилегания к подлежащим образованиям. В биологических трансплантатах необходимо делать перфорационные отверстия, которые способствуют более быстрому прорастанию и замещению пластической ткани собственными тканями больного. Немаловажное значение в исходе операции имеют минимальная травматизация сшиваемых тканей, надежный гемостаз, асептичность, использование ареактивного шовного материала
Описанный способ пластики задней стенки пахового канала в большинстве случаев является достаточно надежным методом лечения сложных паховых грыж. Исключение составляют гигантские косые грыжи с выпрямленным каналом, а также многократно рецидивирующие грыжи. В этом случае, как правило, возникает необходимость в радикальной реконструкции всех стенок пахового канала и его отверстий. Нами разработан способ операции при наличии таких сложных грыж, отличительной чертой которого является наиболее рациональное использование пластического материала, что позволяет без значительного усложнения техники операции создать искусственный паховый канал с прочными стенками и отверстиями должного диаметра.
Тоскин К.Д., Жебровский В.В. Грыжи живота, 1983г.
Источник
