Лапароскопические операции при диафрагмальных грыжах

Техника лапароскопической операции при грыже пищеводного отверстия диафрагмы.Пациент должен быть подготовлен для лапароскопического доступа также, как и для открытого, на случай, если возникнет необходимость перейти к открытой операции. Пневмоперитонеум накладывают так же, как описано для холецистэктомии. Пациента укладывают на спину на операционном столе в обратном положении Тренделенбурга с наклоном 20° для лучшего обзора кардиоэзофагеальной зоны. Для выполнения операции необходимо ввести 5 троакаров с канюлями диаметром 10 мм. Один троакар следует разместить по средней линии, приблизительно на 5 см выше пупка, другой вводят приблизительно на 5 см ниже мечевидного отростка, следующий троакар размещают по левой среднеключичной линии на расстоянии приблизительно 4-5 см от реберной дуги, еще один троакар размещают по левой стороне на уровне пупка. Последний троакар накладывают по правой среднеключичной линии на расстоянии примерно 5 см от реберной дуги. Лапароскоп с угловой оптикой в 30-45″ одновременно с видеокамерой продвигают через супраумбиликальную канюлю. Верхнюю срединную и левую подреберную среднеключичную канюли используют для введения инструментов, выделения пищеводного отверстия диафрагмы и работы хирурга. Через правую подреберную среднеключичную канюлю вводят ретрактор для левой доли печени. Чаще всего используют ретрактор, раскрывающийся как веер и фиксирующийся в одной позиции в течение всей операции. Левую латеральную канюлю используют для введения удерживаемых ассистентом инструментов, чтобы осуществить тракцию желудка по направлению книзу. Троакар, используемый для введения лапароскопа и видеокамеры, вводят первым. Четыре остальных троакара вводят под визуальным контролем. Следует ввести назогастральный зонд 18 F, а также мягкий буж (50 F) Hurst или Maloney так, чтобы его дистальный конец находился в нижней трети пищевода, и можно было при необходимости продвинуть его в желудок.
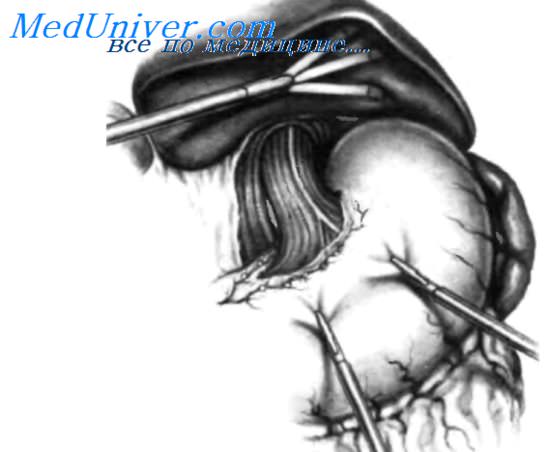
Чтобы приподнять левую долю печени, ретрактор вводят через правую подреберную среднеключичную канюлю, после чего он расправляется веером. Этот ретрактор фиксируют на месте, чтобы ассистенту не нужно было удерживать его в течение всей операции. Двумя атравматическими зажимами осуществляют тракцию передне-верхней стенки желудка. При поднятии левой доли печени и тракции желудка вниз кардиопищеводная зона становится доступной обзору. Брюшину, покрывающую переднюю стенку пищевода, разделяют с помощью изогнутых ножниц или конусовидного крючка для электрокаутеризации. Для того чтобы освободить правый край пищевода, необходимо пересечь с помощью электрокаутеризации проксимальную часть желудочно-печеночной связки, начиная с рыхлой части. При разделении плотной части желудочно-печеночной связки следует разыскать аберрантную левую печеночную артерию, чтобы сохранить ее и предотвратить некроз левой доли печени. Если аберрантная левая печеночная артерия найдена, ее не следует лигировать. Освобожден правый край пищевода, видна правая ножка диафрагмы. Для выделения задней стенки пищевода очень полезен суперэластичный диссектор с меняющейся кривизной. Передний блуждающий нерв, который прилежит к передней стенке пищевода, обычно сохраняют, также как и задний, граничащий справой ножкой диафрагмы. Дистальныи отдел пищевода мобилизован. Мобилизованы также фундальныи отдел желудка и верхняя часть большой кривизны, чтобы можно было подготовить 360° манжету для «окутывания» пищевода без натяжения. Мобилизацию свода желудка выполняют, пересекая желудочно-диафрагмальную связку с помощью электрокаутеризации. Затем переднюю стенку желудка захватывают атравматическим зажимом около большой кривизны на уровне селезенки и осуществляют аккуратную тракцию вправо для выделения коротких сосудов желудка. Короткие сосуды лигируют клипсами, накладывая для большей надежности по две клипсы на каждый край, как можно видеть на рисунке. Короткие сосуды следует выделить, перевязать и пересечь по отдельности. Обычно для освобождения 15 см фундального отдела и большой кривизны от угла Гиса необходимо лигировать три или четыре верхних коротких сосуда. На рисунке показано пересечение четырех наиболее проксимальных коротких сосудов с двумя клипсами на каждой стороне.
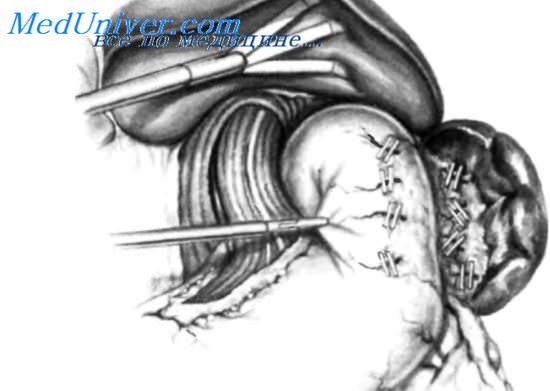
Сигарообразный дренаж Penrose проведен вокруг нижнего отдела пищевода для осуществления тракции пищевода влево, что позволяет увидеть пищеводное отверстие диафрагмы и закрыть его узловыми нерассасывающимися швами. Для того чтобы стало возможным провести сигарообразный дренаж вокруг пищевода, правый угловой зажим необходимо ввести через подготовленную заранее гибкую канюлю. Зажим продвигают позади пищевода, захватывают конец сигарообразного дренажа и проводят его вокруг дистального отдела пищевода. Тракцию осуществляют за концы сигарообразного дренажа, который выведен наружу через небольшой прокол в брюшной стенке. На рисунке показано, что пищевод отведен влево и пищеводное отверстие диафрагмы ушивают узловыми швами. Швы следует накладывать, оставляя 10 мм между краем пищевода и наиболее проксимальным швом. Ушивание следует производить с введенным назогастральным зондом 18 F.
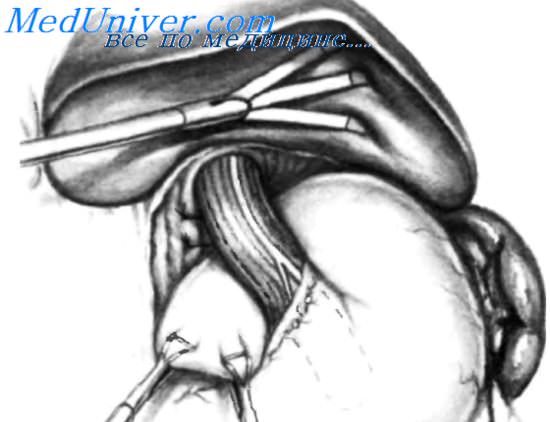
На рисунке показано, что фундальныи отдел желудка проведен позади дистального сегмента пищевода для продолжения фундопликации по Nissen. Чтобы провести фундальныи отдел вокруг пищевода, справа позади пищевода проводят зажим ВаЬсоск. Другим зажимом ВаЬсоск или зажимом Glassman осуществляют тракцию за фундальныи отдел, проводя его за пищеводом. На рисунке показано, что тракция фундального отдела осуществляется двумя зажимами ВаЬсоск, проведенными позади пищевода. Когда фундальныи отдел проведен позади пищевода, назогастральный зонд оттягивают назад проксимальнее и мягкий буж, который был оставлен в ди-стальной трети пищевода, вводят в желудок. Буж не следует вводить в желудок до проведения фундального отдела желудка вправо во избежание затруднений при формировании фундопластики. Прошивают обе желудочные складки. Обычно накладывают два нерассасывающихся шва, чтобы захватить на одной стороне серозно-мышечный слой левой желудочной складки, затем мышечный слой пищевода и, наконец, серозно-мышечный слой правой желудочной складки. Некоторые хирурги используют три или четыре шва. Однако не стоит выполнять фундопликацию высотой более 3 см из-за часто развивающейся после этого дисфагии. Когда прошивание желудка завершено, мягкий буж удаляют и повторно вводят назогастральныи зонд. Чтобы подтвердить степень сужения, получившегося при фундопликации, используют зонд диаметром 5 мм. Он должен легко проводиться между стенкой пищевода и фундопликацией. – Также рекомендуем “Язвы желудка. Классификация язв желудка.” Оглавление темы “Резекция пищевода. Язвы желудка.”: |
Источник

Все материалы на сайте подготовлены специалистами в области хирургии, анатомии и профильных дисциплинах.
Все рекомендации носят ориентировочный характер и без консультации лечащего врача неприменимы.
Грыжа пищеводного отверстия диафрагмы (ГПОД, или грыжа пищевода, диафрагмальная грыжа) – довольно распространенная патология, по статистике встречается у 30% больных с заболеваниями желудочно-кишечного тракта. Формируется при сочетании нескольких патологических условий:
- Неполноценность соединительной ткани (за счет чего происходит растяжение отверстия диафрагмы больше нормы).
- Длительное повышение брюшного давления (тяжелая физическая работа, запоры, вздутие живота, асцит и т.д.).
В результате через растянутое отверстие в диафрагме происходит выпячивание некоторых органов из брюшной полости в грудную. Чаще всего – это часть верхнего отдела желудка. Реже такое неправильное положение может занимать большая часть желудка или часть кишечника.

В норме место перехода пищевода в желудок (по другому оно называется кардией) находится в брюшной полости и крепится к диафрагме особой пищеводно- диафрагмальной связкой. Слева от кардии располагается дно желудка, медиальная часть которого составляет с пищеводом острый угол (угол Гиса). Сохранение этого острого угла очень важно для нормального функционирования пищеводно-желудочного соединения.
При грыже часть кардиального отдела желудка выпячивается вместе с покрывающей его брюшиной и располагается сбоку от пищевода (параэзофагальная грыжа), или же брюшная часть пищевода вместе с прилегающей частью желудка впячивается в грудную полость (скользящая диафрагмальная грыжа).
Как проявляется ГПОД
В большинстве случаев ГПОД являются случайной находкой при рентгенографии или эндоскопическом исследовании. Такие бессимптомные грыжи не требуют лечения, пациенту только рекомендуется изменение режима питания и образа жизни для профилактики осложнений.
Но пищеводная грыжа может доставлять пациенту немало неприятных симптомов – изжогу, дискомфорт и боли за грудиной, нарушение прохождения твердой пищи, отрыжку. Однако в большинстве случаев пищеводная грыжа лечится консервативно путем корректировки питания и образа жизни, назначения противовоспалительных препаратов и блокаторов кислотности. При этом сама грыжа остается, но уходят симптомы.
И только в 20% случаев при такой грыже может быть предложена операция.
В каких же случаях такие пациенты передаются хирургам?

гастроэзофагальный рефлюкс
Грыжи внушительных размеров, в результате которых происходит сдавление органов грудной клетки.
- Неэффективность нескольких курсов консервативной терапии при наличии таких осложнений, как эзофагит, гастроэзофагальный рефлюкс, язвенная болезнь.
- В случаях, когда под влиянием грыжи нарушается проходимость пищи (сужение пищевода, деформация желудка).
- Анемия, обусловленная грыжей (возникающая из-за микрокровотечений, а также нарушения всасывания железа и витамина В12).
Подготовка к операции
Операции при грыжах пищевода обычно плановые, проводятся после тщательного обследования и подготовки. Не очень часто выполняются экстренные операции при осложненных грыжах (ущемление, прободение или кровотечение из сдавленного органа).
Основные обследования – это анализы крови и мочи, биохимический анализ крови, исследование свертывающей системы, электрокардиограмма, рентгенография органов грудной клетки, осмотр врача-терапевта. Для уточнения выбора операции и ее объема обязательно проведение фиброэзофагогастроскопии (ФГС), а также обязательным методом исследования грыжи является рентгеноскопия пищевода и желудка.
Противопоказания для операции:
- Острые инфекционные заболевания.
- Обострения хронических болезней.
- Заболевания сердца в стадии декомпенсации.
- Тяжелые заболевания легких с дыхательной недостаточностью.
- Некомпенсированный сахарный диабет.
- Заболевания крови с нарушением свертывания.
- Почечная и печеночная недостаточность.
- Беременность.
- Онкологические заболевания.
- Недавно перенесенные полостные операции.
Основные виды операций при диафрагмальных грыжах

Основные принципы удаления грыжи пищевода – это:
- Установление брюшного отдела пищевода и вышедшей части желудка в обычное положение под диафрагмой.
- Ушивание растянутого отверстия в диафрагме.
- Укрепление пищеводно-диафрагмальной связки.
- Восстановление постоянного острого угла Гиса для предупреждения рефлюкса.
Поскольку диафрагма находится на границе брюшной и грудной полостей, доступ к ее пищеводному отверстию может быть осуществлен как с той, так и с другой стороны. Соответственно и операции по удалению пищеводных грыж разделяются на:
- Абдоминальные (через разрез брюшной полости),
- Торакальные (разрез по межреберьям грудной клетки).
В современной хирургии предпочтение отдается абдоминальному доступу. Лапаротомические операции привычнее, легче, позволяют провести тщательную ревизию брюшной полости, а при необходимости провести лечение сопутствующей патологии ЖКТ (например, холецистэктомию при каменном холецистите). Болевой синдром в послеоперационном периоде менее выражен при абдоминальных операциях.

фундопликация по Ниссену
В нашей стране основной операцией при ГПОД является фундопликация по Ниссену. Операция выполняется доступом через брюшную полость. Суть операции – из стенок верхней части желудка формируется «муфта» вокруг пищеводного сфинктера, стенка желудка затем подшивается или к передней или к задней стенке брюшной полости для создания фиксированного острого пищеводно-желудочного угла.
Все большую популярность набирают лапароскопические операции при грыжах пищевода. Производится 4 прокола в брюшной стенке, вводится лапароскоп и хирургические инструменты. Под контролем эндоскопа производится низведение грыжевого выпячивания в брюшную полость, ушивание растянутого грыжевого отверстия, а также фундопликацию по типу метода Ниссена.
Минимальная хирургическая травматизация и быстрое восстановление после операции – все это делает лапароскопический метод все более привлекательным. По отзывам пациентов, перенесших лапароскопическую коррекцию пищеводной грыжи, уже на следующие сутки после операции отмечается улучшение самочувствия – исчезает постоянная изжога и дискомфорт.
Совсем недавно в нашей стране стал практиковаться также эндоскопический метод лечения пищеводной грыжи без разрезов – путем введения через рот в пищевод специального аппарата Esophyx, с помощью которого формируется острый угол между пищеводом и желудком и манжетка в месте пищеводно-желудочного соустья.
Видео: операция Esophyx – грыжа пищеводного отверстия диафрагмы
Послеоперационный период
В течение нескольких суток в области операционного поля обычно сохраняется отек, который может несколько сужать просвет пищевода и затруднять прохождение пищи. Поэтому несколько дней (иногда до 2-х недель) при глотании может ощущаться дискомфорт. Часто после операции в просвете пищевода оставляют назогастральный зонд на 1-2 суток, через который осуществляется питание больного жидкой пищей.
-
 Первый день рекомендуется только питье воды (до 300 мл). Остальную жидкость вводят путем инфузии солевых растворов в вену.
Первый день рекомендуется только питье воды (до 300 мл). Остальную жидкость вводят путем инфузии солевых растворов в вену. - На вторые сутки разрешается употребить маленькую порцию жидкой пищи (низкокалорийный суп).
- Постепенно порции увеличиваются, добавляются мягкие продукты, с легкостью продвигающиеся по пищеводу.
- Постепенно в течение 2-х месяцев пациент возвращается к обычному питанию.
- Все питье и пища, принимаемые в послеоперационнм периоде, должны быть теплыми (сравнимы с температурой тела), чтобы не вызвать дополнительный отек.
В послеоперационном периоде назначаются антибиотики, обезболивающие препараты, при нарушении моторики желудочно-кишечного тракта – прокинетики (церукал, мотилиум). Швы снимаются на 7-е сутки, после чего пациент выписывается из стационара под наблюдение гастроэнтеролога.
Очень важно после операции исключить факторы, которые могут способствовать рецидив заболевания, а именно:
- Исключить тяжелые физические нагрузки.
- Не переедать.
- Питаться правильно для исключения метеоризма и запоров.
- При необходимости провести лечение заболеваний других органов ЖКТ для нормализации моторики желудка и кишечника.
- Избегать тесных тугих поясов.
- Адекватно лечить бронхолегочные заболевания, чтобы уменьшить хронический кашель.
Возможные осложнения после операции:
- Кровотечение.
- Прободение желудка или пищевода.
- Пневмоторакс.
- Воспаление с развитием перитонита или медиастинита.
- Нарушение проходимости пищевода.
- Рецидив заболевания.
При наличии показаний операция по удалению пищеводной грыжи может быть проведена бесплатно в государственной клинике. В платных клиниках стоимость такой операции колеблется от 60 до 150 тыс. рублей.
Видео: грыжа пищеводного отверстия диафрагмы – медицинская анимация
Видео: грыжа пищеводного отверстия диафрагмы, ГПОД
Источник
Андреев А.Л., Проценко А.В., Глобин А.В., Хирургия. Журнал им. Н.И. Пирогова, 2010, стр. 82-85.
Этиологическими факторами развития посттравматической диафрагмальной грыжи являются открытая или закрытая травма груди и живота, торакоабдоминальное ранение и ятрогенные повреждения [2, 3]. Посттравматическая диафрагмальная грыжа не всегда имеет грыжевой мешок, на основании этого некоторыми авторами предложен термин «ложная грыжа». Однако наличие или отсутствие грыжевого мешка мало отражается на клиническом течении заболевания и лечебной тактике, поэтому термин «посттравматическая диафрагмальная грыжа» прочно вошел в медицинскую литературу [1, 2, 5]. Чаще оказывается поврежденным левый купол диафрагмы [2, 3].
Диагностика посттравматической диафрагмальной грыжи нередко бывает затруднительной, особенно если факт повреждения диафрагмы не был установлен в остром периоде травмы [2—4]. Сложность диагностики диафрагмальной грыжи обусловлена и тем фактом, что это довольно редкое заболевание и врачи недостаточно осведомлены о нем. Наибольшие диагностические трудности возникают при развитии ущемления посттравматической диафрагмальной грыжи и кишечной непроходимости [2].
Вмешательства при заболеваниях и повреждениях диафрагмы относятся к сложным реконструктивным операциям [3]. На результаты хирургического лечения диафрагмальной грыжи влияют доступ и объем операционной травмы, поэтому предлагаются различные способы и доступы для устранения грыжи [2, 3, 5].
В поисках путей улучшения результатов хирургического лечения диафрагмальной грыжи стала применяться эндовидеохирургическая техника [1, 4].
В литературе имеются единичные сообщения о применении лапароскопической техники у этой категории больных [1, 4, 6—8]. Мы посчитали целесообразным опубликовать два наших клинических наблюдения.
Больной X., 40 лет, поступил в клинику 31.03.07 с жалобами на схваткообразные боли в эпигастральной области и по всему животу, вздутие живота, задержку стула и газов. Из анамнеза известно, что в 1995 г. перенес автодорожную травму с переломом VIII—X ребер слева и левосторонним гемотораксом, выполнено дренирование плевральной полости слева. В последующие годы пациенту неоднократно выполнялась флюорография грудной клетки, при которой патологических изменений не выявилось. До поступления в клинику пациента периодически беспокоили боли в эпигастральной области с иррадиацией в спину, в связи с чем неоднократно выполнялась фиброгастродуоденоскопия. Эти боли объясняли наличием гастрита и купировали противоязвенной и спазмолитической терапией. 28.03 после физической нагрузки появились аналогичные боли, не купирующиеся спазмолитиками, на 3-и сутки присоединились признаки толстокишечной непроходимости. При компьютерной томографии грудной клетки и брюшной полости выявлено, что выше диафрагмы слева на фоне ткани легкого определяется полый орган, заполненный газом, в брюшной полости — раздутые петли тонкой и толстой кишки с уровнями жидкости (рис. 1). Диагностирована посттравматическая левосторонняя диафрагмальная грыжа, осложненная ущемлением и толстокишечной непроходимостью.

Рис. 1. Компьютерные томограммы грудной клетки и брюшной полости больного Х. Посттравматическая лево-сторонняя диафрагмальная грыжа, осложненная ущемлением и толстокишечной непроходимостью.
а — поперечный срез; б, в — продольные срезы соответственно в прямой и боковой.
31.03 больной оперирован. Лапароскопическое вмешательство выполняли под общей комбинированной внутривенной анестезией с интубацией трахеи и искусственной вентиляцией легких с адекватной миоплегией. На операционном столе положение больного на спине. Для улучшения доступа к диафрагме основные этапы операции выполняли с приподнятым на 20—25° головным концом операционного стола и его наклоном на 15—20° влево. Операцию проводили с использованием стандартного эндовидеохирургического комплекта аппаратуры и инструментов. В брюшную полость ввели 3 троакара. 1-й (10 мм) — пo средней линии по середине расстояния между пупком и мечевидным отростком, 2-й (5 мм) — по средней линии у мечевидного отростка, 3-й — по среднеключичной линии справа ниже реберной дуги. При осмотре отметили незначительное количество серозного выпота в боковых отделах брюшной полости и малого таза, раздутые подвздошную и правую половину ободочной кишок. В левом куполе диафрагмы обнаружили дефект и ущемленные в нем поперечную ободочную кишку ближе к левому изгибу и участок большого сальника, окруженные рубцовыми сращениями (рис. 2, а). Следующим этапом выполнили лапароскопический адгезиолизис, объем которого ограничили зоной оперативного вмешательства. Электрохирургическим крючком в радиальных направлениях надсекли ущемляющее кольцо грыжевых ворот и тракциями низвели в брюшную полость ущемленную ободочную кишку и прядь большого сальника, одновременно рассекая спайки. Особо тщательно выделяли ущемленную поперечную ободочную кишку, остерегаясь повреждения стенки этого органа. После низведения ущемленных органов в брюшную полость развился пневмоторакс, в связи с чем давление в брюшной полости снизили до 7—8 мм рт.ст. В левом куполе диафрагмы имелся окруженный рубцовой тканью дефект размером 2×3,5 см, через который просматривалась плевральная полость и ткань левого легкого (рис. 2, б). После освобождения дефекта диафрагмы от рубцовой ткани его ушили отдельными узловыми двухрядными швами нерассасывающейся нитью (рис. 2, в). После оценки жизнеспособности ранее ущемленных органов произвели резекцию большого сальника, а странгуляционную борозду кишки перитонизировали отдельными серо-серозными швами. Резецированный сальник удалили из брюшной полости в контейнере. На завершающем этапе выполнили гемостаз в зоне вмешательства и в левое поддиафрагмальное пространство установили контрольный дренаж. В плевральную полость в седьмом межреберье по переднеподмышечной линии ввели дренаж и наладили постоянную аспирацию. На следующий день после операции после контрольной рентгенографии грудной клетки удалили дренажи из плевральной и брюшной полостей. Послеоперационный период протекал без осложнений. Самостоятельный стул на 2-й день после операции, активизация больного на 3-и сутки. Больной выписан на 4-е сутки после операции. На контрольных рентгенограммах через 2 мес и 2 года дефектов в левом куполе диафрагмы нет, положение ее в нормальной анатомической позиции.

Рис. 2. Интраоперационные фотографии.
а — дефект левого купола диафрагмы с ущемленными в нем толстой кишкой и прядью большого сальника; б, в — начальный и завершающий этапы ушивания дефекта диафрагмы.
Больной В., 46 лет, поступил в клинику 21.04.08 с жалобами на периодические схваткообразные боли в эпигастральной области, сопровождающиеся задержкой стула и вздутием живота, которые разрешались после приема касторового масла и спазмолитиков. В декабре 2007 г. получил проникающее ранение левой половины грудной клетки с повреждением левого желудочка сердца и множественными ранениями легкого, сопровождающимися острой тампонадой сердца, гемопневмотораксом слева, а также колото-резаную рану поясничной области слева; были диагностированы шок II—III степени, посттравматический перикардит. Больной экстренно оперирован. Были выполнены торакотомия слева, резекция нижней доли левого легкого, перикардотомия, диагностическая лапароскопия. При торакальной операции и диагностической лапароскопии повреждения диафрагмы обнаружено не было. Ретроспективно можно предположить, что у пациента имело место незамеченное или непроникающее ранение левого купола диафрагмы, которое в дальнейшем вследствие физической нагрузки и разницы давлений в брюшной и плевральной полостях привело к образованию посттравматической диафрагмальной грыжи. При поступлении на рентгенограммах в прямой и боковой проекциях выявлен дефект левого купола диафрагмы, а выше него слева на фоне ткани легкого определяется полый орган, заполненный газом (рис. 3, а, б). Диагностирована посттравматическая левосторонняя диафрагмальная грыжа. Предложена операция, от которой больной отказался и выписался из клиники. 06.05 появились схваткообразные боли в животе, тошнота, рвота съеденной пищей, задержка стула и газов. 07.05 больной повторно госпитализирован. На основании данных обследования диагностирована ущемленная посттравматическая диафрагмальная грыжа слева, острая толстокишечная непроходимость (рис. 3, в). 08.05 — операция. Доступы, хирургическая находка и техника лапароскопического вмешательства были при мерно такие же, как в предыдущем клиническом наблюдении. На следующий день послеоперационного периода после рентгенологического контроля грудной клетки и брюшной полости удалены дренажи из плевральной и брюшной полостей. Самостоятельный стул у пациента был на 2-й день после операции. 11.05 пациент выписан из стационара. На контрольной рентгенограмме через 7 мес дефектов левой половины диафрагмы нет (рис. 4). В настоящее время состояние пациента хорошее, работает по специальности.

Рис. 3. Рентгенограмма грудной клетки в прямой (а) и боковой (б) проекциях и брюшной полости (в) больного В.
Посттравматическая левосторонняя диафрагмальная грыжа, осложненная ущемлением и толстокишечной непроходимостью.

Рис. 4. Рентгенограммы грудной клетки в прямой (а) и боковой (б) проекциях больного В. через 7 мес. После операции.
Наглядной демонстрацией «закона парных случаев» является редкое заболевание —левосторонняя посттравматическая диафрагмальная грыжа, которая приводит к ущемлению и острой толстокишечной непроходимости.
Таким образом, при наличии у больных клинической карти ны нарушения кишечной проходимости в сочетании с анамнестическими указаниями на травму с возможным повреждением диафрагмы целесообразно рекомендовать обязательный диагностический поиск посттравматической диафрагмальной грыжи.
Лапароскопия наряду с рентгенологическим исследованием и компьютерной томографией является дополнительным методом диагностики посттравматической диафрагмальной грыжи, позволяющим выработать оптимальную хирургическую тактику лечения в конкретном клиническом наблюдении.
Лапароскопическая хирургия — это безопасный, эффективный, малотравматичный метод лечения больных с посттравматической диафрагмальной грыжей, осложненной ущемлением и толстокишечной непроходимостью. Лечение диафрагмальной грыжи лапароскопическим методом по сравнению с традиционной операцией имеет преимущества: меньшая травматичность и болезненность, косметический эффект, значительное сокращение срока временной нетрудоспособности, быстрое восстановление физической активности, меньшее число осложнений.
При лапароскопическом устранении посттравматической диафрагмальной грыжи закономерно развивается пневмоторакс. Перед его возникновением необходимо предупредить об этом анестезиолога и снизить давление в брюшной полости до 5—7 мм рт.ст.
В процессе лапароскопического устранения посттравматической диафрагмальной грыжи, осложненной ущемлением и кишечной непроходимостью, хирург должен быть готов в любой момент перейти на традиционную открытую операцию.
ЛИТЕРАТУРА
1. Андреев А.Л., Проценко А.В., Глобин А.В. Лапароскопическая хирургия диафрагмальной грыжи. Эндоскоп хир 2009; 1: 89.
2. Котив Б.Н. Диафрагмальные грыжи травматического происхождения. Торакальная хирургия. Под ред. Л.М. Бисенкова. Ст-Петербург: Гиппократ 2004; 1812—1818.
3. Пищик В.Г., Яблонский П.К., Козак А.Р. и др. Правосторонняя посттравматическая диафрагмальная грыжа с полной эвентрацией печени в правую плевральную полость. Медицина. XXI век 2009; 1: 81—82.
4. Baldassarre Е., Valenti G., Gambino M. et al. The role of laparoscopy in the diagnosis and the treatment of missed diaphragmatic hernia after penetrating trauma. J Laparoendosc Adv Surg Tech A 2007; 17: 3: 302—306.
5. Crandall M., Popowich D., Shapiro M., West M. Posttraumatic hernias: historical overview and review of the literature. Am Surg 2007; 73: 9: 845—850.
6. Cueto J., Vazquez-Frias J.A., Nevarez R. et al. Laparoscopic repair of traumatic diaphragmatic hernia. Surg Laparosc Endosc Percutan Tech 2001; 11: 3: 209—212.
7. Matthews B.D., Bui H., Harold K.L. et al. Laparoscopic repair of traumatic diaphragmatic injuries. Surg Endosc 2003; 17: 2: 254—258.
8. Meyer G., Huttl T.P., Hatz R.A., Schildberg F.W. Laparoscopic repair of traumatic diaphragmatic hernias. Surg Endosc 2000; 14: 11: 1010—1014.
Источник